题目内容
【题目】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)氧化剂_____,还原剂_____;
(2)反应中转移电子数是_____;
(3)氧化剂与氧化产物的质量比_____;
(4)当生成2.8gN2时,被氧化的物质的质量是____g。
【答案】Cl2 NH3 6e- 213:28 3.4g
【解析】
分析反应8NH3+3Cl2=6NH4Cl+N2可知,NH3中的N元素由-3价部分升高到N2中的0价,但NH4Cl中N元素价态不变。Cl元素由0价降低到-1价。
(1) Cl元素由0价降低到-1价,所以Cl2是氧化剂。答案为Cl2。
N元素由-3价升高到0价,所以NH3是还原剂。答案为NH3。
(2)从Cl2看,3Cl2共得电子6e-。答案为6e-
(3)氧化剂为Cl2,氧化产物为N2,二者的质量比为3×71:28=213:28,答案为213:28
(4)当生成2.8gN2时,被氧化的物质为NH3,其质量是![]() 。
。
答案为3.4g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
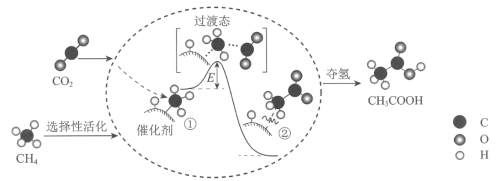
小学生10分钟应用题系列答案【题目】中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。在适当的条件下,将CO2转化为甲醇、甲醚等有机物,既可降低CO2造成的温室效应对环境的影响,还可得到重要的有机产物。
(1)已知T K时,某恒容密闭容器中存在如下反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
c(CO2) | c(H2) | c(CH3OCH3) | c(H2O) | |
开始时 | a | b | 0 | 0 |
10 s时 | 3 | 0.5 | c | 1.5 |
①若T K时,化学平衡常数K=15,则10 s 时v(正)_______v(逆)(填“>”“<”或“=”),此时CO2的转化率为________。
②既能提高反应速率,又能提高H2转化率的方法是___________(填序号)。
A.加入过量CO2气体 B.升高温度 C.适当压缩容器体积 D. 将CH3OCH3(g) 分离出去
(2)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生的反应为CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=50 kJ·mol1。
CH3OH(g)+H2O(g) ΔH=50 kJ·mol1。
①下图1中能表示该反应的平衡常数K与温度T之间的变化关系曲线为______(填“a”或“b”),其判断依据是__________________________________。
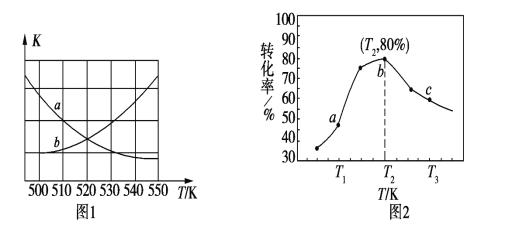
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如图2所示,则在该时间段内,恰好达到化学平衡时,容器内的压强与反应开始时的压强之比为____________。