题目内容
【题目】在 K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2+7H2O反应中。
(1)______元素被氧化
(2)此反应若转移了12mol的电子,则生成氯气______L(标准状况)
【答案】Cl 134.4
【解析】
由方程式可知,反应中Cr从+6价降低到+3价,得到电子,发生还原反应,Cl从-1价升高到0价,发生氧化反应,且电子转移6mol时被氧化的HCl为6mol,据此计算。
(1)由分析可知Cl元素被氧化;
(2)电子转移6mol时被氧化的HCl为6mol,生成氯气3mol,因此反应若转移了12mol的电子,生成氯气6mol,体积为6mol×22.4L/mol=134.4L。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是

选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A. A B. B C. C D. D
【题目】研究氮的氧化物具有重要意义。回答下列问题:
(1)2016年10月19日“天宫二号”与“神舟十一号”顺利实现太空交会对接。运载火箭用的是一种叫肼(N2H4)的燃料和氧化剂NO2,两者反应生成氮气和气态水。
已知: N2 (g) + 2O2 (g) = 2NO2 (g) △H = +67.7 kJ·mol-1
N2 H4 (g) +O2 (g) = N2 (g) +2H2 O (g) △H =-543 kJ·mol-1
①写出肼和NO2反应的热化学方程式__________________________________。
②若已知: 2H2(g)+O2(g)=2H2O(g) ΔH1=-Q1 kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH2=-Q2 kJ·mol-1,
则 Q1_________Q2(填“>”“<”或“=”)。
(2)汽车尾气净化器中发生的反应为2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。一定条件下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2CO2(g)。一定条件下,在三个体积均为1.0 L恒容密闭容器中发生上述反应,测得有关实验数据如下:
容器 | 温度/(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 |
| 0.12 |
II | 400 | 0.4 | 0.4 | 0 | 0 |
| x |
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 |
|
①容器I中达到平衡所需时间2 s,则v(N2)=_______;
②x_____0.24(填“>”、“=”、“<”);△H_____0 (填“>”、“=”、“<”);
③若起始时向I中充入NO、CO各0.1 mol,N2、CO2各0.0 5 mol,开始时v(正)
___ v(逆) (填“>”、“=”、“<”)。
(3)SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
①SCR(选择性催化还原)工作原理:

尿素溶液浓度影响NO2的转化,控制尿素的浓度非常关键。测定溶液中尿素(M=60 g·mol 1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的V1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用V2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是________________________。
②NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。
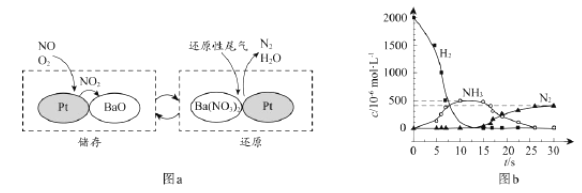
通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是_______;
用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__________。


