题目内容
4.图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是NH4++OH-=NH3+H2O.
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:

①X、Y与水混合后反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓.
②N→⑦的单质反应的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
③若将Y溶液加热蒸干、灼烧后得到的物质的化学式是Al2O3.
分析 由元素在周期表中位置,可知①为H、②为C、③为N、④为O、⑤为F、⑥为Na、⑦为Al、⑧为Cl.
(1)N元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物硝酸铵;电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大;③、④、⑤元素的氢化物均含氢键,但水中氢键数目多,F的非金属性最强;
(2)均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,为铵根离子与氢氧根离子反应生成氨气与水的反应;
(3)元素⑦的单质为Al,可推知N为氧化铝、Z为氢氧化铝,电解熔融氧化铝得到Al与氧气,X、Y含有一种相同元素,其中X焰色反应呈黄色,故X溶液为NaAlO2,Y溶液是氯化铝,以此来解答.
解答 解:由元素在周期表中位置,可知①为H、②为C、③为N、④为O、⑤为F、⑥为Na、⑦为Al、⑧为Cl.
(1)N元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物硝酸铵;电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,离子半径Cl->O2->Na+>Al3+;③、④、⑤元素的氢化物均含氢键,但水中氢键数目多,F的非金属性最强③、④、⑤元素的氢化物的沸点由高到低的顺序是H2O>HF>NH3,故答案为:硝酸铵;Cl->O2->Na+>Al3+;H2O>HF>NH3;
(2)均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,为铵根离子与氢氧根离子反应生成氨气与水的反应,离子反应为NH4++OH-=NH3+H2O,
故答案为:NH4++OH-=NH3+H2O;
(3)元素⑦的单质为Al,可推知N为氧化铝、Z为氢氧化铝,电解熔融氧化铝得到Al与氧气,X、Y含有一种相同元素,其中X焰色反应呈黄色,故X溶液为NaAlO2,Y溶液是氯化铝,则
①X、Y与水混合后反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
②N→⑦的单质反应的化学方程式为2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑,故答案为:2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑;
③若将Y(氯化铝)溶液加热水解生成氢氧化铝和HCl,HCl挥发,蒸干得到氢氧化铝,灼烧后得到的物质的化学式是Al2O3,故答案为:Al2O3.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素化合物性质为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不大.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案| A. | 滤纸上有Ag,Cu,Fe滤液中有Fe2+,Mg2+ | |
| B. | 滤纸上有Ag,滤液中有Fe2+,Cu2+,Mg2+,Ag+ | |
| C. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+ | |
| D. | 滤纸上有Ag,Cu,滤液中有Fe2+,Cu2+,Mg2+,Ag+ |
| 物质 | 组成和结构信息 |
| 甲 | 含有非极性共价键的常见二元离子化合物 |
| 乙 | 含有极性键和非极性键的18e-分子 |
| 丙 | 化学组成为BE,熔点高,可作超硬耐磨涂层材料 |
| 丁 | 化学组成为DBA4的离子化合物 |
(1)D+的结构示意图为
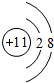 ;
;(2)C、D、E的氢化物按熔点由高到低排列的顺序为NaH>H2O>PH3;
(3)乙属于极性分子(填“极性”或“非极性”),丁的电子式为
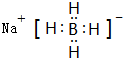 ,
,(4)将少量甲投入到AlCl3溶液中反应的离子方程式为6Na2O2+4Al3+6H2O=4Al(OH)3↓+3O2↑+12Na+;
(5)氮化硼晶体的熔点要比丙晶体高,其原因是磷原子半径比氮原子大,N-B共价键键长比B-P小,则N-B键能大.
| A. | Na+ | B. | CO32ˉ | C. | CH3COO- | D. | NH4+ |
| A. | 将X、Y分别通入品红溶液中,均使品红溶液褪色 | |
| B. | 将X、Y分别通入氢硫酸中,只有Y能产生沉淀 | |
| C. | 等物质的量的X、Y同时通入品红溶液中,品红溶液不褪色 | |
| D. | 等物质的量的X、Y同时通入BaCl2溶液中,有沉淀产生 |
| A. | 若a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| B. | 若a1=a2,b1=2b2,则混合溶液中c(CH3COO-)>c(CH3COOH)>c(Na+) | |
| C. | 若a1b1>a2b2,则混合液的pH一定大于7 | |
| D. | a1=a2,且混合溶液的pH<7,则b1一定大于b2 |

 A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).
A、B、C、D、E、F是初中化学常见的六种物质,其中A和B、C和D组成的元素种类相同,它们之间的转化关系如图所示((图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,图中已略去部分物质).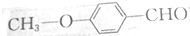 )的同分异构体既能发生银镜反应,又能与FeCl3溶液发生显色反应的有13种.
)的同分异构体既能发生银镜反应,又能与FeCl3溶液发生显色反应的有13种.