题目内容
【题目】用NA表示阿伏伽德罗常数的值,下列叙述不正确的是( )
A.标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA
B.通常状况下,8g O2和O3 的混合气体含有的分子数是0.5NA
C.常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl﹣ 个数为0.4NA
D.标准状况下,11.2L H2在氧气中完全燃烧后得到的产物的分子数为0.5NA
【答案】B
【解析】解:A.氧气和氮气都是双原子分子,标准状况下,6.72LO2和N2的混合气体物质的量 ![]() =0.3mol,含有原子物质的量为0.6mol,含有的原子数为0.6NA , 故A正确;
=0.3mol,含有原子物质的量为0.6mol,含有的原子数为0.6NA , 故A正确;
B.氧气和臭氧摩尔质量不同,所以相同质量的氧气和臭氧物质的量不同,含有的分子数不同,故B错误;
C.常温常压下,2mol/L的100mL MgCl2溶液中含有氯化镁含有物质的量为2mol/L×0.1L=0.2mol,含有Cl﹣ 个数为0.2mol×2NA=0.4NA , 故C正确;
D.标准状况下,11.2L H2物质的量为 ![]() =0.5mol,依据2H2+O2=2H2O,可知在氧气中完全燃烧后得到的产物的分子数为0.5NA , 故D正确;
=0.5mol,依据2H2+O2=2H2O,可知在氧气中完全燃烧后得到的产物的分子数为0.5NA , 故D正确;
故选:B.

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案【题目】2013年9月以来,我国很多地区再大面积出现雾霾,特别是华中华北尤其严重,汽车尾气、燃煤废气和冬季取暖排放的CO2等都是形成雾霾的原因。
Ⅰ.用于净化汽车尾气的反应为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
(1)能判断该反应达到平衡状态的标志是_______。
A.在单位时间内生成1mol CO2的同时消耗了1mol CO
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再变化
(2)在t2时刻将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件.请在图中补充画出从t2到t4时刻正反应速率随时间的变化曲线:___________

Ⅱ.使用石油热裂解的副产物CH4来制取H2,其生产流程如图1所示:
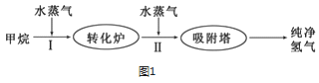
(3)此流程的第Ⅰ步反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)
CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)

(4)此流程的第Ⅱ步反应的平衡常数随温度的变化情况如下表
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
从表上可以推断该反应是___________(填“吸热”或“放热”)反应,若反应在500℃时进行,设CO(g)和H2O(g)的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为________;
(5)图3表反应Ⅱ在t1时达到平衡,在t2时因改变某个条件引起浓度变化的情况,图中t2时改变的条件是降低温度或________________(写一种)
【题目】下列实验设计的步骤及现象均正确的是( )
选项 | 实验目的 | 实验步骤及现象 |
A | 证明氯水有酸性 | 试样 |
B | 检验某红棕色气体是否为溴蒸气 | 试样 |
C | 证明酸性条件下H2O2氧化性比 I2强 | NaI |
D | 比较: Ksp(AgCl)>Ksp(AgI) | AgNO3 溶液 |
A. A B. B C. C D. D
