题目内容
如图所示,把试管小心地放入盛有(20 ℃)碳酸饮料的烧杯中,试管中开始放入适量饱和CuSO4溶液,再用滴管滴加5 mL浓硫酸于试管中,试回答下列问题:

(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)试管中破坏化学键的类型是______________,形成的化学键类型是______________。
(4)写出有关现象的化学方程式______________。
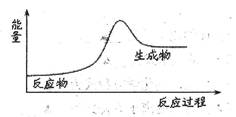
(5)由实验推知,反应所得溶液的总能量__________(填“大于”、“小于”或“等于”)浓硫酸和饱和CuSO4溶液的总能量。

(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)试管中破坏化学键的类型是______________,形成的化学键类型是______________。
(4)写出有关现象的化学方程式______________。
(5)由实验推知,反应所得溶液的总能量__________(填“大于”、“小于”或“等于”)浓硫酸和饱和CuSO4溶液的总能量。
(1)烧杯中有大量气泡冒出,小试管中析出固体
(2)浓硫酸溶于饱和CuSO4溶液放热,使饮料温度升高,碳酸分解,CO2溶解度降低而逸出,饱和CuSO4溶液因浓H2SO4吸水而析出CuSO4·5H2O
(3)共价键 离子键、共价键
(4)H2CO3===H2O+CO2↑ (5)小于
(2)浓硫酸溶于饱和CuSO4溶液放热,使饮料温度升高,碳酸分解,CO2溶解度降低而逸出,饱和CuSO4溶液因浓H2SO4吸水而析出CuSO4·5H2O
(3)共价键 离子键、共价键
(4)H2CO3===H2O+CO2↑ (5)小于
浓硫酸稀释放出大量的热,使烧杯中碳酸饮料温度升高,二氧化碳受热溶解度降低,这样使碳酸分解,破坏碳酸中共价键,从而又形成H2O和CO2中的共价键,逸出大量CO2气泡冒出,浓硫酸吸水,使饱和CuSO4溶液中析出晶体,从而形成了CuSO4中的离子键。

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
 2CO2 2H2+O2
2CO2 2H2+O2 CO2+2H2O
CO2+2H2O 2SO3为放热反应,关于该反应的下列说法正确的是( )。
2SO3为放热反应,关于该反应的下列说法正确的是( )。 3CO2+4H2O。下列说法中不正确的是( )
3CO2+4H2O。下列说法中不正确的是( )