��Ŀ����
����Ŀ�����������Na2O2������CO2�ų�O2�����ó�������(KO2)����Na2O2Ҳ����ͬ�������á�
��1��д��KO2��CO2�ķ�Ӧ����ʽ________________________________.
��2��lkgNa2O2��lkgKO2���ֱ��CO2��Ӧ�����ɵ�O2�����(ͬ��ͬѹ��)Ϊ__________��
��3�������ʵ�����CO2�ֱ���������Na2O2��KO2��Ӧ���ɵ�O2�����(ͬ��ͬѹ��)Ϊ__________��
��4������Ϊѡ��_______________����������Ϊ���ʣ�������_____________��
���𰸡� 4KO2+2CO2�T2K2CO3+3O2 71��117����0.6��1�� 1��3 KO2 ��Ϊ��KO2�ͷ�������Ч�ʸ���
�����������������������֪����������г�������(KO2) �ɴ���Na2O2����CO2�ų�O2��
��1��KO2��CO2�ķ�Ӧ����ʽΪ4KO2+2CO2�T2K2CO3+3O2.
��2��lkgNa2O2��CO2��Ӧ���������������ʵ���Ϊ![]() mol��lkgKO2��CO2��Ӧ�������������ʵ���Ϊ
mol��lkgKO2��CO2��Ӧ�������������ʵ���Ϊ![]() mol���������ɵ�O2���ʵ���֮��Ϊ
mol���������ɵ�O2���ʵ���֮��Ϊ![]() ����ͬ��ͬѹ��������ȵ��������ʵ���֮����
����ͬ��ͬѹ��������ȵ��������ʵ���֮����
��3��1mol CO2�ֱ���������Na2O2��KO2��Ӧ���ɵ�O2�����ʵ����ֱ�Ϊ0.5mol��1.5mol��������ͬ��ͬѹ���������������������Ϊ1��3 ��
��4�����������ݿ�֪��ѡ��KO2��Ϊ�����������ʣ���������KO2�ͷ�������Ч�ʸ�����

 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�����Ŀ�����и����ĸ������ʣ������������ת�����ǣ� �� 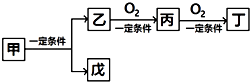
���� | �� | �� | �� | �� | �� |
A | C6H12O6 | CH3CH2OH | CH3CHO | CH3COOH | CO2 |
B | NH4Cl | NH3 | N2 | NO2 | HCl |
C | NaCl | Na | Na2O | Na2O2 | Cl2 |
D | CH4 | C | CO | CO2 | H2 |
A.A
B.B
C.C
D.D