题目内容
下列说法正确的是
A.常温下pH=12的NaOH溶液,与等体积0.01mol·L一l氯化铵溶液混合后所得溶液中:c(Na+)=c(NH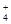 )
)
B.新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.室温下,向0.0lmol/L NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO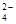 )>c(NH
)>c(NH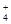 )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
D.物质的量浓度均为0.lmol/L的NaA和NaB棍合溶液中,粒子浓度的关系一定为:c(Na+)>c(OH-)>c(HA)>c(HB)
C
解析试题分析:A、等浓度的NaOH和NH4Cl反应,得到的NH4+会发生水解,不相等,错误;B、根据浓度大小:c(H+)>c(Cl-)> >c(OH-)>c(ClO-),错误;C、NH4HSO4和NaOH按1:1混合时,溶液呈酸性,因此NaOH需要过量,正确;D、不能确定A、B离子的强弱,因此无法判断,错误。
考点:本题考查了溶液中离子的大小关系,溶液中的守恒关系等知识。

 阅读快车系列答案
阅读快车系列答案某一元有机酸HA的溶液中,若未电离的HA分子个数与溶液中的离子个数比为a:b,则HA的电离度(即转化率)是
A.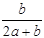 ×100% ×100% | B. ×100% ×100% |
C.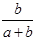 ×100% ×100% | D.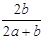 ×100% ×100% |
下列叙述正确的是( )
| A.在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变 |
| B.Na2CO3溶液加水稀释后再恢复至原温度, pH和KW均减小 |
| C.室温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水电离出的c(H+)之比104:1 |
| D.25℃,若测知氨水与NH4Cl混合溶液的pH>7,则溶液中c(NH4+)>c(Cl—) |
已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1L0.2mol·L-1HF溶液中加入1L0.2mol·L-1CaCl2溶液,则下列说法中,正确的是
| A.25℃时,0.lmol·L-1溶液中pH=l |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中没有沉淀产生 |
| D.该体系中HF与CaC12反应产生沉淀 |
用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度不变,下列各项中始终保持增大趋势的是
| A.c(CH3COOH) | B.c(H+) |
C. | D.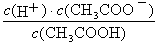 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
25℃下,下列有关说法正确的是
A.浓度为0.1mol/L的HCN溶液中c(OH-)=10-13mol/L
B.物质的量浓度相同的稀酸溶液中KW:CH3COOH>H2CO3>HCN
C.物质的量浓度相同的三种钠盐溶液的pH:NaHCO3>NaCN>CH3COONa
D.浓度均为amol?L-1HCN溶液与NaOH溶液等体积混合充分反应后的溶液中(忽略体积的变化)c(H+)<c(OH-)<c(CN-)<0.5amol/L
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列叙述正确的是 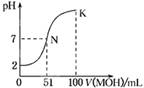
| A.HA为弱酸,MOH为强碱 |
| B.pH=7时,HA与MOH恰好完全反应 |
| C.在N点,c(A-)=c(M+) + c(MOH) |
| D.在K点,c(M+)>c(A-)>c(OH-)>c(H+) |
SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是
| A.Na2SO3溶液中存在:c(Na+)>c(SO32-)>c(H2SO3)>c(HSO3-) |
| B.已知NaHSO3溶液pH<7,该溶液中:c(Na+)>c(HSO3-)>c(H2SO3) >c(SO32-) |
| C.当吸收液呈中性时:c(Na+)=2 c(SO32-)+c(HSO3-) |
| D.当吸收液呈酸性时:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3) |