题目内容
15.某一元醇8g与足量的金属钠完全反应,在标准状况下得到2.8L氢气.该物质可能是( )| A. | CH3OH | B. | C2H5OH | C. | C3H7OH | D. | C4H9OH |
分析 金属与醇反应,醇中-OH中的氢原子被还原生成氢气,根据H原子守恒可知,n(一元醇)=2n(H2),根据n=$\frac{V}{Vm}$计算氢气的物质的量,再根据M=$\frac{m}{n}$计算一元醇的摩尔质量,据此结合选项判断.
解答 解:标准状况下得到2.8L 氢气的物质的量为$\frac{2.8L}{22.4L/mol}$=0.125mol,所以n(一元醇)=2n(H2)=2×0.125mol=0.25mol,故该一元醇的摩尔质量为$\frac{8g}{0.25mol}$=32g/mol.
A、CH3OH摩尔质量为32g/mol,故A正确;
B、C2H5OH摩尔质量为46g/mol,故B错误;
C、C3H7OH摩尔质量为60g/mol,故C错误;
D、C4H9OH摩尔质量为74g/mol,故D错误.
故选:A.
点评 考查有机物分子式的确定,比较基础,判断氢气与一元醇的物质的量关系是关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.在下列各组溶液中,离子一定能大量共存的是( )
| A. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| C. | FeCl3溶液:K+、Na+、SO42-、AlO2- | |
| D. | 含0.1mol/LNH4Al(SO4)2的溶液:K+、Ca2+、HCO3-、Cl- |
3.某酸性溶液中,下列离子能够大量共存的是( )
| A. | Fe3+ SCN-Na+ NO${\;}_{3}^{-}$ | B. | Cu2+ SO${\;}_{4}^{2-}$HCO${\;}_{3}^{-}$K+ | ||
| C. | CO${\;}_{3}^{2-}$Na+Cl-K+ | D. | Ba2+ Ca2+ Cl-NO${\;}_{3}^{-}$ |
10.下列变化属于化学变化的是( )
| A. | 分镏 | B. | 裂解 | C. | 蒸馏 | D. | 萃取 |
4.下列实验能获得成功的是( )
| A. | 用溴水鉴别苯、CCl4、乙烯 | |
| B. | 加浓溴水,然后过滤除去苯中的少量己烯 | |
| C. | 用苯、溴水、铁屑混合制取溴苯 | |
| D. | 用分液法分离乙醇和乙酸乙酯 |
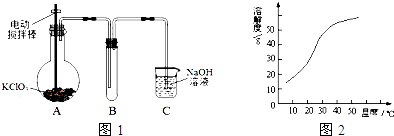
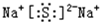 ,化合物BA2的结构式是:S=C=S;
,化合物BA2的结构式是:S=C=S;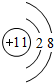 .
.