题目内容
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:H2O>NH3>SiH4
B.氢元素与另外一种元素可形成共价化合物或离子化合物
C.S、Cl的含氧酸的酸性依次增强
D.用中文“![]() (ào)”命名的第118号元素在周期表中位于第七周期0族
(ào)”命名的第118号元素在周期表中位于第七周期0族
【答案】C
【解析】
A.非金属性越强,氢化物越稳定,非金属性O>N>Si,气态氢化物的稳定性:H2O>NH3>SiH4,故A正确;
B.H与F、Cl等形成共价化合物,与Na等活泼金属可以形成离子化合物,则氢元素与其他元素可形成共价化合物或离子化合物,故B正确;
C.S、Cl的含氧酸不一定是最高价含氧酸,因此酸性不一定依次增强,如硫酸为强酸,次氯酸为弱酸,故C错误;
D.目前周期表中各周期可以容纳的元素种类,118号元素在周期表中位于第七周期0族,故D正确;
故选C。

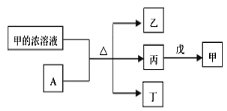
【题目】苯甲醛在碱性条件下可发生反应: 2C6H5CHO + NaOH→C6H5CH2OH+C6H5COONa。相关物质的物理性质如下表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |||
溶 解 性 | 水中 | 微溶 | 微溶 | 温度 | 溶解度 | 不溶 |
17℃ | 0.21 g | |||||
25℃ | 0.34 g | |||||
100℃ | 5.9 g | |||||
有机溶剂中 | 易溶 | 易溶 | 易溶 | 易溶 | ||
密度(20℃)/g·cm-3 | 1.0 | 1.0 | 1.3 | 0.9 | ||
沸点/℃ | 178 | 205 | 249 | 80 | ||
熔点/℃ | 26 | -15 | 122 | 5.4 | ||
制备苯甲醇和苯甲酸的实验流程及涉及的主要实验装置(部分加热和固定装置已略)如下:
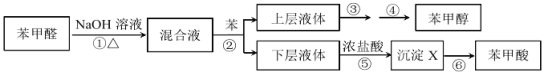
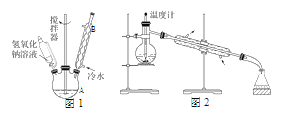
(1)第①步所用装置(如图 1),用搅拌器的目的是______________。仪器 B 的作用是_______________。
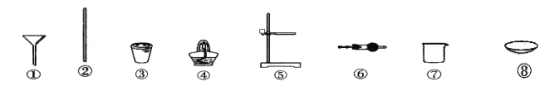
(2)第②步所用玻璃仪器有烧杯、_______________。
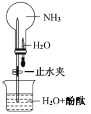
(3)第③步采用沸水浴加热蒸馏,收集到的馏分为_________;再进行第④步,操作如图 2 所示。图 2 中有一处明显错误,正确的应改为_________________________。
(4)第⑤步反应的离子方程式为________________________________________; 冷水洗涤沉淀 X 的优点是_________________________;检验沉淀 X 洗涤干净与否的操 作:______________。
(5)第⑥步经过滤、洗涤、干燥得苯甲酸产品,然后用电子天平准确称取 0.2440 g 苯甲酸样品于锥形瓶中,加 100 mL 蒸馏水溶解,再用 0.1000 mol·L-1 的标准 NaOH 溶液 进行滴定,经平行实验,测得消耗 NaOH 溶液的平均值为 19.20 mL,则苯甲酸样品的纯 度为_________ (质量百分数)。