题目内容
(1)只用一种试剂(2)不用任何试剂及仪器就可以确定以下各种等物质的量浓度的溶液中pH由小到大的顺序,其顺序是
A、NaClB、CH3COONaC、NaHSO4 D、Na2CO3E、NaClO
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:当它们pH相同时,其物质的量浓度由大到小的排列是
分析:(1)鉴别出Na2CO3、NaOH、AgNO3、Na2S及NaNO3,其中硝酸钠无法通过试剂直接鉴别;其它各物质,碳酸钠一般通过生成气体鉴别、氢氧化钠通过生成难溶氢氧化物鉴别、硝酸银溶液需要通过生成银的难溶物鉴别、硫化钠可以利用硫离子具有的还原性鉴别;
(2)根据各溶液的酸碱性先进按照酸性、中性、碱性的顺序分组,然后再根据盐的水解情况比较溶液的pH大小;
(3)醋酸为弱电解质,溶液中部分电离,盐酸为一元强酸,硫酸为二元强酸,若pH相同时,溶液中氢离子浓度相同,据此判断三种的物质的量浓度关系;当三种的物质的量浓度相同时,氢离子浓度越小,溶液的pH越大;中和同一碱溶液,需要的氢离子的物质的量相同,根据三种酸中含有的氢离子个数判断需同浓度的三种酸溶液的体积关系.
(2)根据各溶液的酸碱性先进按照酸性、中性、碱性的顺序分组,然后再根据盐的水解情况比较溶液的pH大小;
(3)醋酸为弱电解质,溶液中部分电离,盐酸为一元强酸,硫酸为二元强酸,若pH相同时,溶液中氢离子浓度相同,据此判断三种的物质的量浓度关系;当三种的物质的量浓度相同时,氢离子浓度越小,溶液的pH越大;中和同一碱溶液,需要的氢离子的物质的量相同,根据三种酸中含有的氢离子个数判断需同浓度的三种酸溶液的体积关系.
解答:解:(1)Na2CO3、NaOH、AgNO3、Na2S及NaNO3五瓶无色溶液,可以使用氯化铁溶液进行鉴别:碳酸钠与氯化铁反应生成红褐色沉淀和气体、氢氧化钠与氯化铁生成红褐色沉淀、硝酸银与氯化铁生成白色沉淀、硫化钠与氯化铁溶液反应生成硫单质,且氯化铁溶液褪色、硝酸钠与氯化铁溶液没有明显现象,
故答案为:FeCl3(aq);
(2)A、NaCl B、CH3COONa C、NaHSO4 D、Na2CO3E、NaClO中,显示酸性的有:C、NaHSO4;显示中性的为:A、NaCl;显示碱性的为:B、CH3COONa、D、Na2CO3 E、NaClO;显示碱性的三种物质都为强碱弱酸盐,根据“越弱越水解”可知,水解程度增大,碱性最强的为D、Na2CO3 ,其次为E、NaClO,水解程度最小,碱性最弱的是B、CH3COONa,所以各溶液的pH大小关系为:C<A<B<E<D,
故答案为:C<A<B<E<D;
(3)①CH3COOH、②HCl、③H2SO4三种溶液,当它们pH相同时,要求溶液中氢离子浓度相同,醋酸为弱电解质,只能部分电离出氢离子,所以醋酸的浓度最大,其次是盐酸为一元强酸、硫酸为二元强酸,所以氯化氢浓度大于硫酸,即物质的量浓度由大到小的排列是①>②>③;
当它们的物质的量浓度相同时,溶液在氢离子浓度越大,溶液的pH越小,所以醋酸中氢离子浓度最小,溶液pH最大,其次是盐酸为一元酸,氢离子浓度小于硫酸,盐酸的pH大于硫酸,所以pH大小关系为:①>②>③;
中和同一烧碱溶液,根据中和反应实质,需要氢离子的物质的量相等,由于三种酸溶液同浓度,且醋酸、盐酸为一元酸、硫酸为二元酸,所以需要三种溶液的体积关系为:①=②=2③,
故答案为:①>②>③; ①>②>③; ①=②=2③.
故答案为:FeCl3(aq);
(2)A、NaCl B、CH3COONa C、NaHSO4 D、Na2CO3E、NaClO中,显示酸性的有:C、NaHSO4;显示中性的为:A、NaCl;显示碱性的为:B、CH3COONa、D、Na2CO3 E、NaClO;显示碱性的三种物质都为强碱弱酸盐,根据“越弱越水解”可知,水解程度增大,碱性最强的为D、Na2CO3 ,其次为E、NaClO,水解程度最小,碱性最弱的是B、CH3COONa,所以各溶液的pH大小关系为:C<A<B<E<D,
故答案为:C<A<B<E<D;
(3)①CH3COOH、②HCl、③H2SO4三种溶液,当它们pH相同时,要求溶液中氢离子浓度相同,醋酸为弱电解质,只能部分电离出氢离子,所以醋酸的浓度最大,其次是盐酸为一元强酸、硫酸为二元强酸,所以氯化氢浓度大于硫酸,即物质的量浓度由大到小的排列是①>②>③;
当它们的物质的量浓度相同时,溶液在氢离子浓度越大,溶液的pH越小,所以醋酸中氢离子浓度最小,溶液pH最大,其次是盐酸为一元酸,氢离子浓度小于硫酸,盐酸的pH大于硫酸,所以pH大小关系为:①>②>③;
中和同一烧碱溶液,根据中和反应实质,需要氢离子的物质的量相等,由于三种酸溶液同浓度,且醋酸、盐酸为一元酸、硫酸为二元酸,所以需要三种溶液的体积关系为:①=②=2③,
故答案为:①>②>③; ①>②>③; ①=②=2③.
点评:本题考查了未知物检验、弱电解质的电离、越大水解原理应用等知识,题目难度中等,注意掌握盐的水解原理,明确溶液酸碱性与pH大小的关系.

练习册系列答案
相关题目
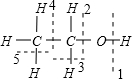 ,则乙醇完全燃烧时,可能不断裂的键是:
,则乙醇完全燃烧时,可能不断裂的键是: ②CH2=CH2 ③CH≡CH ④
②CH2=CH2 ③CH≡CH ④ ⑤
⑤
 ⑦
⑦ 中属于芳香烃的是
中属于芳香烃的是