题目内容
【题目】金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为____________。
(2)Ti能与B、C、N、O等非金属元素形成稳定的化合物,B、C、N的电负性由大到小的顺序为_____;C、N、O的第一电离能由大到小的顺序为_____________。
(3)N的氢化物常作制冷剂,原因是______________。
(4)月球岩石—玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。
SO42-的空间构型为_______形。其中硫原子采用_________杂化,写出SO42-的一种等电子体的化学式:______。
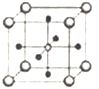
(5)Ti、Ca、O相互作用能形成如图晶体结构(Ti4+位于立方体的顶点、Ca2+位于立方体体心),该晶体的化学式为________。Ti4+和周围_____个O2-相紧邻。该晶胞的边长为apm,则其密度为______g/cm3。
【答案】 1s22s22p63s23p63d24s2 N>C>B N>O>C NH3分子键能形成氢键,沸点较高,以液化,故能够做制冷剂 正四面体 sp3 ClO4- CaTiO3 12 136/(6.02·a3)×107g/cm3
【解析】(1)Ti的原子核外有22个电子,根据电子的排布规律可知基态Ti原子的核外电子排布为1s22s22p63s23p63d24s2或[Ar]3d24s2;(2)根据元素电负性的比较,同周期中的元素,随核电荷数的增加,电负性增强,所以电负性N>C>B;第一电离能随核电荷数的增加而增大,但N的最外层的轨道是半充满状态,比较稳定,所以第一电离能N>O>C;(3)NH3分子间能形成氢键,沸点较高,易液化,故能够做制冷剂;(4)SO42-中的S原子的价层电子对数是![]() ,无孤对电子,所以硫酸根离子的空间构型是正四面体型;其中S采取的是sp3杂化;原子数和价电子数分别都相等的是等电子体,则SO42-的一种等电子体的化学式为ClO4-等。(5)Ti4+位于立方体的顶点,个数是8×1/8=1,Ca2+位于立方体体心,共计1个,氧原子位于面心处,个数6×1/2=3,因此该晶体的化学式为CaTiO3。每层的Ti4+都与4个O2-紧邻,所以该晶体中Ti4+和周围的12个O2-紧邻;该晶胞的边长为apm,则其晶胞的体积是(a×10-10cm)3,所以密度为
,无孤对电子,所以硫酸根离子的空间构型是正四面体型;其中S采取的是sp3杂化;原子数和价电子数分别都相等的是等电子体,则SO42-的一种等电子体的化学式为ClO4-等。(5)Ti4+位于立方体的顶点,个数是8×1/8=1,Ca2+位于立方体体心,共计1个,氧原子位于面心处,个数6×1/2=3,因此该晶体的化学式为CaTiO3。每层的Ti4+都与4个O2-紧邻,所以该晶体中Ti4+和周围的12个O2-紧邻;该晶胞的边长为apm,则其晶胞的体积是(a×10-10cm)3,所以密度为![]() g/cm3。
g/cm3。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】C、N、S对应的化合物,是重要的化学物质。试回答下列问题:
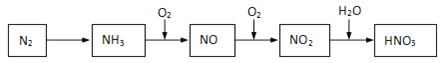
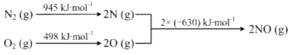
(1)已知:氢气的燃烧热为286.0kJ/mol,氨气的燃烧热为382.5 kJ/mol ,则合成氨反应的热化学方程式
为_____________________。
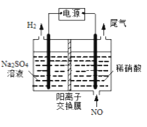
(2)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理。已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为________________。
(3)用活性炭还原法处理氮氧化物。 有关反应为C(s)+2NO(g) ![]() N2(g)+CO2(g)。
N2(g)+CO2(g)。
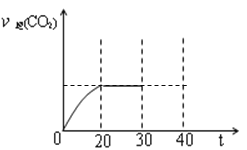
某研究小组向密闭的真空容器中(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T)条件下反应,反应进行到不同时间测得各物质的浓度如表:
时间(min) 浓度(molL-1) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为_________________。
②根据表中数据,计算T℃时该反应的平衡常数为Kp=___________,(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留两位小数)
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率_________(填“增大”“不变”或“减小”)。
④该反应达到平衡时下列说法正确的是______填序号字母)。
a.容器内压强保持不变 b.2v(NO)=v(N2)
c.容器内CO2的体积分数不变 d.混合气体的密度保持不变
⑤30min时改变某一条件,过一段时间反应重新达到平衡,则改变的条件可能是______。请在图中画出30~40min的变化曲线______。