题目内容
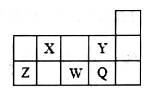
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子最外层电子数之和与Ca2+的核外电子数相等,Y、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
| A.原子半径:Z>Y>X | B.Z与X在同一周期 |
| C.氢化物的稳定性:X>Y | D.XZ4属于共价化合物 |
D
试题分析:3种元素的原子最外层电子数之和与Ca2+的核外电子数相等,应为18,Y、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构,应分别为F、Cl,则X的最外层电子数为4,应为C元素,
A.原子半径应为Cl>C>F,故A错误;B.由以上分析可知X和Z分别位于周期表第二周期和第三周期,故B错误;C.非金属性C<F,氢化物的稳定性:C<F,故C错误;D.XZ4为CCl4,为共价化合物,故D正确.故选D.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 的说法,错误的是
的说法,错误的是