题目内容
己知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ/moL;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ/moL.则HCN在水溶液中电离的△H等于( )A.-67.7kJ/moL
B.-43.5kJ/moL
C.+43.5kJ/moL
D.+67.7kJ/moL
【答案】分析:HCN(aq)与NaOH(aq)反应可分为两步:①HCN在水溶液中电离HCN H++CN;②产生的H+与NaOH(aq)反应;利用盖斯定律进行计算,可得HCN在水溶液中电离的反应热.
H++CN;②产生的H+与NaOH(aq)反应;利用盖斯定律进行计算,可得HCN在水溶液中电离的反应热.
解答:解:反应的热化学方程式分别为:
HCN(aq)+OH-(aq)═CN-(aq)+H2O(l)△H=-12.1kJ?mol-1…①
H+(aq)+OH-(aq)═H2O(l)△H=-55.6kJ?mol-1…②
用①-②可得HCN电离的热化学方程式为:HCN(aq)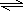 H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,
H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,
故选:C.
点评:本题考查反应热的计算,本题难度不大,做题时注意盖斯定律的应用.
 H++CN;②产生的H+与NaOH(aq)反应;利用盖斯定律进行计算,可得HCN在水溶液中电离的反应热.
H++CN;②产生的H+与NaOH(aq)反应;利用盖斯定律进行计算,可得HCN在水溶液中电离的反应热.解答:解:反应的热化学方程式分别为:
HCN(aq)+OH-(aq)═CN-(aq)+H2O(l)△H=-12.1kJ?mol-1…①
H+(aq)+OH-(aq)═H2O(l)△H=-55.6kJ?mol-1…②
用①-②可得HCN电离的热化学方程式为:HCN(aq)
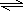 H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,
H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,故选:C.
点评:本题考查反应热的计算,本题难度不大,做题时注意盖斯定律的应用.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目