题目内容
16.下列有关离子键,共价键的叙述中正确的是( )| A. | 离子化合物中只存在离子键,没有共价键 | |
| B. | 共价化合物分子中一定不存在离子键 | |
| C. | 构成单质的粒子中一定含有共价键 | |
| D. | 仅由非金属元素组成的化合物中一定不含离子键 |
分析 A.离子化合物中一定含有离子键,可能含有共价键;
B.只含共价键的化合物是共价化合物;
C.构成单质的粒子中可能不含化学键;
D.仅由非金属元素组成的化合物中可能含有离子键.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH等,故A错误;
B.只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,故B正确;
C.构成单质的粒子中可能不含化学键,如稀有气体,故C错误;
D.仅由非金属元素组成的化合物中可能含有离子键,如铵盐,故D错误;
故选B.
点评 本题考查化学键和物质的关系,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,采用举例法分析解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列有关化学用语正确的是( )
| A. | -OH的电子式: | B. | 丁烷是键线式: | ||
| C. | 乙烯的结构简式:CH2=CH2 | D. | 最能反映甲烷真实结构的模型是: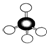 |
7.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2LCCl4中含有的分子数为0.5NA | |
| B. | 1molCl2完全溶于水,转移的电子数为NA | |
| C. | 25℃时,PH=13的1.0LBa(OH)2溶液中含有的OH-数为0.1NA | |
| D. | 电解精炼铜,转移2NA个电子时,阳极溶解64g铜 |
4.常温下,下列各组离子或分子在指定溶液中一定能大量共存的是( )
| A. | 饱和氯水中:Na+、NH4+、S2-、CO32- | |
| B. | 空气中:NO、SO2、H2S、HCl | |
| C. | Fe(OH)3胶体中:Na+、Ag+、Br-、NO3 | |
| D. | 能使甲基橙变红的溶液中:Fe2+、Al3+、SO42-、Cl- |
11.一定条件下,用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )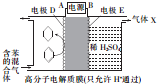

| A. | 电子流向:D→A,B→E | |
| B. | 气体X为O2 | |
| C. | 电极D为惰性电极,E为活泼电极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-═C6H12 |
8.用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落.下列关于上述实验现象的解释不正确的是( )
| A. | 铝在空气中能很快形成氧化膜 | B. | 用酸处理时未能将氧化膜溶解 | ||
| C. | 氧化铝的熔点比铝高 | D. | 氧化铝薄膜包住了熔化的铝 |
6.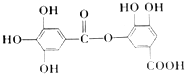 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
 有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )
有一种有机化合物,其结构简式如图所示,下列有关它的性质的叙述中,正确的是( )| A. | 有弱酸性,1mol该有机物与溴水反应,最多能消耗4mol Br2 | |
| B. | 在一定条件下,1mol该物质最多能与6mol NaOH完全反应 | |
| C. | 在Ni催化下,1mol该物质可以和7mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |