题目内容
【题目】向一定量的Fe、FeO、Fe2O3的混合物中,加入500 mL 1 mol/L的盐酸,恰好使混合物完全溶解,放出672 mL(标准状况)气体。向所得溶液中加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能得到铁( )
A. 28 g B. 14 g
C. 12.32 g D. 条件不足,无法计算
【答案】B
【解析】
加入盐酸恰好使混合物完全溶解,向所得的溶液中加入硫氰化钾溶液,无血红色出现,说明溶液中不存在Fe3+,只有Fe2+,即溶液为FeCl2溶液,根据元素守恒分析解答。
根据题意,混合物完全溶解后所得溶液中加入KSCN溶液无血红色出现,可判断原混合物恰好溶于500mL1mol/L的盐酸且反应后的溶液中无Fe3+存在,因此Fe元素在溶液中只以FeCl2的形式存在,溶液中氯离子与亚铁离子的个数比为2:1,n(HCl)=0.5L×1mol/L=0.5mol,则n(FeCl2)=![]() ,n(Fe)= n(FeCl2)=0.25mol,根据Fe元素守恒可知,还原相同质量的此混和物可得到铁的质量m(Fe)=0.25mol×56g/mol=14g,故合理选项是B。
,n(Fe)= n(FeCl2)=0.25mol,根据Fe元素守恒可知,还原相同质量的此混和物可得到铁的质量m(Fe)=0.25mol×56g/mol=14g,故合理选项是B。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】已知某化学反应的平衡常数表达式为K=![]() ,在不同的温度下该反应的
,在不同的温度下该反应的
平衡常数如表所示
t ℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述正确的是( )
A. 该反应的化学方程式是: H2(g)+CO2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
B. 上述反应的正反应是吸热反应
C. 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,如果此时测得CO2为0.5 mol,则该反应达到平衡状态
D. 某温度下,如果平衡常数符合下列关系式: ![]() =
=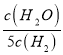 ,则此时温度700℃
,则此时温度700℃
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
【题目】某小组同学为探究 H2O2、 H2SO3、 Br2 氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:
实验操作 | 实验现象 | |
① | 打开活塞 a,滴加氯水,关闭活塞 a | _____________________________________________ |
② | 吹入热空气一段时间后停止 | A中溶液颜色明显变浅;B中有气泡,产生大量白色沉淀,沉降后上层清液为无色 |
③ | 打开活塞b,逐滴加入H2O2溶液 | 开始时溶液颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙红色。 |
完成下列填空:
(1)在进行操作①时,A中的实验现象是___________,有关反应的离子方程式是___________。
(2)操作②吹入热空气的目的是____________。B 中产生白色沉淀的化学式是___________。
(3)装置C的作用是____________________。
(4)由上述实验可知,在此实验条件下,H2O2、H2SO3、Br2氧化性强弱顺序为________________。
(5)操作③开始时颜色无明显变化可能原因是(写出一条即可):___________________。