题目内容
【题目】1 mol某烃在足量的氧气中完全燃烧,生成水和二氧化碳各6 mol,则该烃的分子式为________ ;若该烃能使溴水褪色,在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为 ________________________;写出该烃在催化剂作用下发生加聚反应的化学方程式: ______________。;若该烃不能使溴水褪色,但一定条件下能跟溴发生取代反应,其一溴取代物只有一种,则该烃的结构简式为________________________
【答案】C6H12 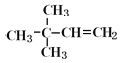
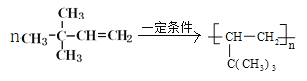
【解析】
0.1mol某烃在足量的氧气中完全燃烧,生成水和二氧化碳各0.6mol,则该烃分子中N(C)=![]() =6、N(H)=
=6、N(H)=![]() =12,则该烃分子式为C6H12;若该烃能使溴水褪色,该烃在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,含有1个C=C双键,则该烃为
=12,则该烃分子式为C6H12;若该烃能使溴水褪色,该烃在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,含有1个C=C双键,则该烃为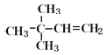 ;若该烃不能使溴水褪色,不含不饱和键,但一定条件下能跟纯溴发生取代反应,其一溴取代物只有一种,则该烃为环己烷,据此解答。
;若该烃不能使溴水褪色,不含不饱和键,但一定条件下能跟纯溴发生取代反应,其一溴取代物只有一种,则该烃为环己烷,据此解答。
0.1mol某烃在足量的氧气中完全燃烧,生成水和二氧化碳各0.6mol,则该烃分子中N(C)=![]() =6、N(H)=
=6、N(H)=![]() =12,则该烃分子式为C6H12;若该烃能使溴水褪色,该烃在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,含有1个C=C双键,则该烃为
=12,则该烃分子式为C6H12;若该烃能使溴水褪色,该烃在催化剂作用下,与H2发生加成反应,生成2,2-二甲基丁烷,含有1个C=C双键,则该烃为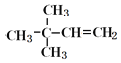 ,名称为3,3-二甲基-1-丁烯,发生加聚反应的方程式为
,名称为3,3-二甲基-1-丁烯,发生加聚反应的方程式为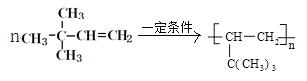 ;若该烃不能使溴水褪色,不含不饱和键,但一定条件下能跟纯溴发生取代反应,其一溴取代物只有一种,则该烃为环己烷,结构简式为
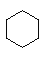
;若该烃不能使溴水褪色,不含不饱和键,但一定条件下能跟纯溴发生取代反应,其一溴取代物只有一种,则该烃为环己烷,结构简式为![]() 。
。

【题目】氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
(1)工业上利用N2和H2可以合成NH3,NH3又可以进一步制备肼(N2H4)等.已知:
N2(g)+2O2(g)=2NO2(g)ΔH=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH=-534.0kJ·mol-1
2NO2(g)![]() N2O4(g)ΔH=-52.7kJ·mol-1
N2O4(g)ΔH=-52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氨气和气态水的热化学方程式________;
(2)在固定体积密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g)ΔH<0,其平衡常数K与温度T的关系如下表:
2NH3(g)ΔH<0,其平衡常数K与温度T的关系如下表:
T/K | 298 | 398 | 498 |
平衡常数K | 4.1×105 | K1 | K2 |
①该反应的平衡常数表达式:K=________;
②判断K1________K2(填写“>”, “=”或“<”);
③下列各项能说明该反应已达到平衡状态的是________(填字母).
a.v(N2)正=3v(H2)逆
b.混合气体的密度保持不变
c.容器内压强保持不变
d.容器内N2、H2、NH3的浓度之比为1︰3︰2
e.N2和H2的转化率相等
f.体系中气体的平均摩尔质量不再改变
(3)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的![]() ,则该温度下的化学平衡常数K=________(保留两位小数),以NH3表示该过程的反应速率v(NH3)=________;
,则该温度下的化学平衡常数K=________(保留两位小数),以NH3表示该过程的反应速率v(NH3)=________;
(4)实验室制取氨气的化学反应方程式________。