题目内容
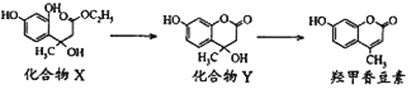
【题目】碱式碳酸镁和无水氯化镁具有广泛用途。用白云石(CaCO3 MgCO3)为原料生产碱式碳酸镁和无水氯化镁的流程如下:
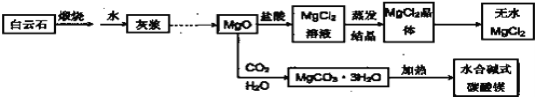
回答下列问题:
(1)“灰浆”中除水和MgO外,主要成分还有:_________________。
(2)为探究所制得的水合碱式碳酸镁(m MgCO3n Mg(OH)2 xH2O )的组成。某同学组装仪器如图所示:
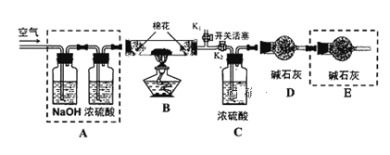
实验测得:硬质玻璃管中剩余的固体质量为1.60g,C处浓H2SO4增重0.72g,D处碱石灰增重1.32g,此水合碱式碳酸镁的化学式为:_______________________。
(3)A框中装置的作用是_____________________________________。
(4)在装好试剂后,加热前应进行的操作是___________________________________。
【答案】Ca(OH)2 3MgCO3·Mg(OH)2·3H2O 除去空气中的水蒸气和CO2等酸性气体 关闭K2,打开K1,通入足量空气后,再打开K2,关闭K1
【解析】
(1)碳酸钙、碳酸镁分解得到氧化钙、氧化镁,氧化钙能与水反应,据此判断;
(2)根据反应的方程式计算;
(3)根据空气中含有水蒸气和二氧化碳分析;
(4)根据需要排除空气中水蒸气和二氧化碳的干扰分析。
(1)碳酸钙、碳酸镁分解得到氧化钙、氧化镁,氧化钙能与水反应生成氢氧化钙,所以“灰浆”中除水和MgO外,主要成分还有Ca(OH)2;
(2)根据方程式可知
mMgCO3nMg(OH)2xH2O![]() (m+n)MgO+mCO2↑+(n+x)H2O
(m+n)MgO+mCO2↑+(n+x)H2O
40(m+n) 44m 18(n+x)
1.60 1.32 0.72
则![]()
解得m=3、n=1、x=3,因此水合碱式碳酸镁的化学式为3MgCO3·Mg(OH)2·3H2O;
(3)实验需要通过测量装置D内碱石灰的增重,计算生成二氧化碳的质量,通过测量装置C的增重,计算生成的水的质量,二空气中和水蒸气和二氧化碳,所以装置A的作用是除去空气中的水蒸气和CO2等酸性气体;
(4)由于要排除空气中水蒸气和二氧化碳的干扰,所以在装好试剂后,加热前应进行的操作是关闭K2,打开K1,通入足量空气后,再打开K2,关闭K1。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案