题目内容
将一种化学式为R(NO3)x·nH2O的硝酸盐晶体6.05 g溶于水配成500 mL溶液,用石墨棒作为电极材料对此溶液进行电解。当通过电流强度为5 A的电流16.05 min时,溶液中的金属离子已全部放电,且其中一电极增重1.60 g(已知此晶体的摩尔质量为242 g·mol-1)。
则:①x=____________,②R的相对原子质量为____________,③n=____________。
则:①x=____________,②R的相对原子质量为____________,③n=____________。
①2 ②64 ③3
已知“溶液中的金属离子已全部放电,且其中一电极增重1.60 g”,所以R的质量为1.60 g,晶体的物质的量为6.05 g/242 g·mol-1="0.025" mol。所以R的相对原子质量为:1.60/0.025=64。溶液中通过的电量为Q=It=5C/s×16.05 min×60 s/min=4.815×103 C,则电子的物质的量: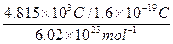 ="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。
="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。
点评:解答本题的思路是根据相关定义展开的。物质的相对原子质量在数值上等于其摩尔质量,所以要求R的相对原子质量需要找物质的质量和其物质的量。从定义出发,看似方法很笨,但是只要基础扎实,解题细心,一样可以很快地解出较难的试题。在高三复习中,应注意定义、概念,注重基础,重视课本,才能帮助自己提高能力,摆脱题海。
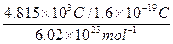 ="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。
="0.05" mol,则每个原子得2个电子,金属为+2价,x=2。n=(242-64-2×62)/18=3。点评:解答本题的思路是根据相关定义展开的。物质的相对原子质量在数值上等于其摩尔质量,所以要求R的相对原子质量需要找物质的质量和其物质的量。从定义出发,看似方法很笨,但是只要基础扎实,解题细心,一样可以很快地解出较难的试题。在高三复习中,应注意定义、概念,注重基础,重视课本,才能帮助自己提高能力,摆脱题海。

练习册系列答案
相关题目
 CuSO4+5H2O,CuSO4
CuSO4+5H2O,CuSO4 CuO+SO3
CuO+SO3 2Cu2O+O2,2SO3
2Cu2O+O2,2SO3 2SO2+O2
2SO2+O2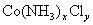 (x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用
(x、y为正整数)。为了确定x和y的值,取两份质量均为0.2140g的该化合物进行如下两个实验。将一份试样溶于水,在硝酸存在的条件下用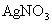 溶液滴定(生成
溶液滴定(生成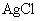 沉淀),共消耗24.0mL 0.100mol/L的
沉淀),共消耗24.0mL 0.100mol/L的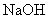 溶液并加热,用足量盐酸吸收逸出的
溶液并加热,用足量盐酸吸收逸出的 。吸收
。吸收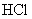 溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)
溶液。试通过计算确定该化合物的化学式。(本题可能用到的相对原子质量:H为1.00、N为14.0、Cl为35.5、Co为58.9)