题目内容
【题目】在某无色酸性溶液中能大量共存的一组离子是( )
A.Na+、K+、HCO3﹣、NO3﹣
B.NH4+、SO42﹣、Al3+、NO3﹣
C.Na+、Ca2+、NO3﹣、CO32﹣
D.K+、MnO4﹣、NH4+、NO3﹣
【答案】B
【解析】解:A.H+与HCO3﹣反应生成CO2而不能大量共存,故A错误;B.酸性条件下,离子之间不发生任何反应,可大量共存,故B正确;
C.酸性条件下,H+与CO32﹣反应生成CO2而不能大量共存,并且CO32﹣与Ca2+反应生成沉淀,故C错误;
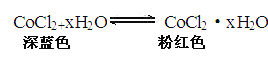
D.MnO4﹣有颜色,不符合题目无色的要求吗,故D错误.
故选B.

【题目】NH3是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
共价键 | 键能/ kJ·mol-1 |
H―H | 436 |
N≡N | 946 |
N―H | 391 |
注:拆开气态物质中1 mol某种共价键需要吸收的能量,就是该共价键的键能。
N2 (g)+3 H2 (g)![]() 2 NH3 (g) H =____kJ·mol-1
2 NH3 (g) H =____kJ·mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2 +3H2 ![]() 2NH3,测得各组分浓度随时间变化如图1所示。
2NH3,测得各组分浓度随时间变化如图1所示。

①表示c(N2)的曲线是__(填“曲线A”、“曲线B”或“曲线C”)。
②0~t0时用H2表示反应速率v(H2)____mol·L-1·min-1。
③下列能说明该反应达到平衡的是____。
a.混合气体的压强不再变化
b.2c(H2)= 3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:

①电极b名称是____。
②电解质溶液中OH-离子向____移动(填“电极a”或“电极b”)。
③电极a的电极反应式为____。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是____。