题目内容
9.下列有关电解原理的说法不正确的是( )| A. | 电解饱和食盐水时,一般用铁作阳极,碳作阴极 | |
| B. | 电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 | |
| C. | 对于冶炼像钠、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 | |
| D. | 电解精炼铜时,用纯铜板作阴极,粗铜板作阳极 |
分析 A.活性电极作阳极时,电极失电子;
B.电镀时,镀层作阳极、镀件作阴极;
C.活泼金属采用电解熔融盐或氧化物的方法冶炼;
D.阴极电解原理分析,电解精炼铜粗铜做阳极,精铜做阴极,含铜离子的电解质溶液.
解答 解:A.活性电极作阳极时,电极失电子,用铁做阳极,铁失电子发生氧化反应,所以电解饱和食盐水时,用石墨作阳极,故A错误;
B.电镀时,阳极上金属失电子发生氧化反应、阴极上金属阳离子得电子发生还原反应生成金属单质,所以镀层作阳极、镀件作阴极,故B正确;
C.活泼金属采用电解熔融盐或氧化物的方法冶炼,冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法,故C正确;
D.用电解法精炼粗铜时用纯铜作阴极,粗铜做阳极,故D正确,
故选A.
点评 本题考查了原电池及电解池原理及金属的冶炼,根据金属的活泼性强弱确定冶炼方法,知道原电池和电解池各个电极上发生的反应,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
20.已知Q与R的摩尔质量分别为18g/mol和44g/mol,在反应X+2Y═2Q+R中,当1.6g X与Y完全反应后,生成4.4gR,则参与反应的Y和生成物Q的质量之比为( )
| A. | 46:9 | B. | 32:9 | C. | 23:9 | D. | 16:9 |
17.1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和8体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
| A. | 乙炔 | B. | 丙烯 | C. | 1,3-丁二烯 | D. | 丙炔 |
4.下列电离方程式书写错误的是( )
| A. | H2SO4=2H++SO42- | B. | Ba(OH)2=Ba2++2OH- | ||
| C. | Na2CO3=2Na+1+CO3-2 | D. | NaHCO3=Na++HCO3- |
14.下列表示物质或微粒的化学用语正确的是( )
| A. | Mg 2+的结构示意图: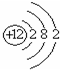 | B. | NH3分子的电子式: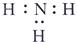 | ||
| C. | H2S的结构式:H-S-H | D. | CH4分子的比例模型: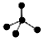 |
1.有一支25mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体放出一部分到bmL刻度线处,盛入量筒内,所得液体体积一定是( )
| A. | (a-b) mL | B. | (25-a)mL | C. | (b-a)mL | D. | 大于a mL |
19.某高分子化合物的结构为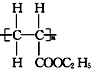 ,下列有关叙述正确的是( )
,下列有关叙述正确的是( )
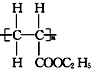 ,下列有关叙述正确的是( )
,下列有关叙述正确的是( )| A. | 其单体是CH2=CH2和HCOOC2H5 | B. | 它是缩聚反应产物 | ||
| C. | 其链节是CH3CH2-COOC2H5 | D. | 其单体是CH2=CH-COOC2H5 |