题目内容
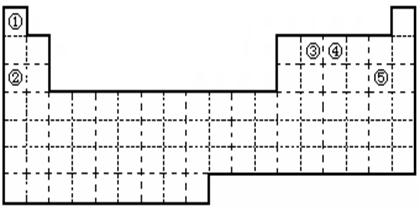
A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),L层电子数是(a+b),则A、B两元素形成的化学式最可能表示为( )
A.B3A2 B.BA2 C.A3B2 D.AB2
A.B3A2 B.BA2 C.A3B2 D.AB2
B
试题分析:因为B的L层电子为(a+b)个且有M层,所以a+b=8,又因A原子最外层电子数为a个,次外层电子数为b个,且满足a+b=8,所以A原子有两个电子层,且K层为2个电子,L层为6个电子。进而推知B的各电子层上的电子数分别为2、8、4。即A为O,B为Si。故本题选B。
点评:本题主要考查原子核外电子的排布规律,结合元素周期表可推测出A、B两元素。题目难度不大。

练习册系列答案
相关题目