题目内容
【题目】下列有关实验操作、现象和解释或结论都正确的( )
选项 | 实验操作 | 现象 | 解释或结论 |
① | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
② | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
③ | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
④ | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
⑤ | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
⑥ | 将H2O2溶液滴入KMnO4溶液中 | KMnO4溶液褪色 | 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O |
⑦ | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
⑧ | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
A.①④⑤⑥⑦B.④⑤⑥C.④⑤⑥⑦D.①⑤
【答案】C
【解析】
根据浓硝酸的强氧化性进行判断;根据Fe3+的检验方法进行判断;根据Ksp大小判断AgCl和AgI溶解性大小;根据氨水显碱性进行判断;根据浓硫酸的脱水性进行判断;根据高锰酸钾的强氧化性进行判断;根据钠和醇反应原理进行判断;根据铁和水蒸气反应原理进行判断。
![]() 过量的Fe粉中加入稀
过量的Fe粉中加入稀![]() ,反应生成硝酸亚铁,则滴入KSCN溶液,溶液不变红,故错误;
,反应生成硝酸亚铁,则滴入KSCN溶液,溶液不变红,故错误;
![]() 沉淀中滴入稀KCl溶液,有白色沉淀出现,可能因为Cl-的浓度过大,导致c(Cl-)c(Ag+)>Ksp(AgCl),理论上AgI更难溶,则不能发生沉淀的转化,故错误;
沉淀中滴入稀KCl溶液,有白色沉淀出现,可能因为Cl-的浓度过大,导致c(Cl-)c(Ag+)>Ksp(AgCl),理论上AgI更难溶,则不能发生沉淀的转化,故错误;
![]() 箔插入稀
箔插入稀![]() 中,发生氧化还原反应生成硝酸铝、NO和水,则观察到固体溶解,气泡冒出,故错误;
中,发生氧化还原反应生成硝酸铝、NO和水,则观察到固体溶解,气泡冒出,故错误;
![]() 浓氨水中一水合氨电离生成
浓氨水中一水合氨电离生成![]() ,显碱性,则玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,故正确;
,显碱性,则玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,故正确;
![]() 将浓硫酸滴到蔗糖表面,变黑与脱水性有关,膨胀是因C与浓硫酸发生氧化还原反应生成气体,所以体现浓硫酸有脱水性和强氧化性,故正确;
将浓硫酸滴到蔗糖表面,变黑与脱水性有关,膨胀是因C与浓硫酸发生氧化还原反应生成气体,所以体现浓硫酸有脱水性和强氧化性,故正确;
![]() 过氧化氢与高锰酸钾发生氧化还原反应,
过氧化氢与高锰酸钾发生氧化还原反应,![]() 符合元素守恒、电子守恒,电荷守恒,故正确;
符合元素守恒、电子守恒,电荷守恒,故正确;
![]() 与乙醇反应生成乙醇钠和氢气,则Na能置换出醇羟基中的氢,故正确;
与乙醇反应生成乙醇钠和氢气,则Na能置换出醇羟基中的氢,故正确;
![]() 水蒸气通过灼热的铁粉,反应生成四氧化三铁和氢气,观察到黑色固体生成,故错误;
水蒸气通过灼热的铁粉,反应生成四氧化三铁和氢气,观察到黑色固体生成,故错误;
所以④⑤⑥⑦符合题意,故C正确;
答案:C。

【题目】氯苯是染料、医药、有机合成的中间体,是重要的有机化工产品。实验室制取氯苯的装置如图所示(加热和固定仪器的装置已略去)。
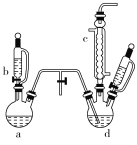
回答下列问题:
(1)如果用a和b仪器组合成制取氯气的装置,反应无需加热,则a仪器中的固体反应物可以是________(填序号)。
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)仪器c的名称是________。
(3)制取氯苯的化学方程式为________________。
(4)仪器d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要进行水洗,其目的是______________________。
(5)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸气,请在下框中画出,并标明所用试剂。
__________
(6)工业生产中苯的流失情况如表所示:
项目 | 二氯苯 | 氯化尾气 | 蒸气 | 成品 | 不确定苯耗 | 合计 |
苯流失量/(kg·t-1) | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
则10 t苯可制得成品氯苯________t。(列出计算式即可。氯苯和苯的相对分子质量分别是112.5和78)
【题目】碱式碳酸铜[Cu(OH)2CuCO3]是一种用途广泛的化工产品,实验室制备碱式碳酸铜的反应原理为:2CuSO4+2Na2CO3+H2O=Cu(OH)2CuCO3↓+CO2↑+2Na2SO4。回答下列问题:
(1)配制100mL浓度均为0.50molL-1的CuSO4溶液和Na2CO3溶液,需要用到的玻璃仪器有量筒、烧杯、胶头滴管和___。
(2)取50mL0.50molL-1CuSO4溶液加入50mL0.50molL-1Na2CO3溶液中,反应后烧杯底部出现大量蓝绿色沉淀。设计实验证明蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4],实验步骤是:过滤,___。
(3)按最佳配比 n(CuSO4)︰n(Na2CO3)=1︰1.2进行实验,反应15min,所得实验结果如下:
温度/℃ | 60 | 65 | 75 | 80 | 90 |
沉淀量/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
分析75℃时沉淀量最多的原因:___。
(4)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2yCuCO3表示。某小组利用以下装置测定某碱式碳酸铜样品的组成:
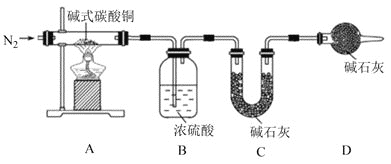
①A中发生反应的化学方程式是___。
②加热时持续通入N2的目的是___。
③称取32.0g样品,充分反应后得到24.0g残留物,B增重3.6g,C增重4.4g。该样品的化学式为___。若对调B和C装置的位置,___(填“能”或“不能”)测算出该样品的化学式。