题目内容
9.在一定条件下,将2mol CO和1mol SO2充入一恒容密闭容器中,发生反应:SO2(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+S(l)△H=-akJ•mol-1,当达到平衡状态时,下列说法中正确的是( )| A. | 生成2mol CO2 | B. | 放出a kJ热量 | C. | CO和CO2共有2mol | D. | 含有3mol氧原子 |
分析 A、可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
B、反应焓变的意义是指反应物按照化学方程式计量数恰好全部反应放出的热量;
C、依据碳元素守恒分析判断;
D、结合氧元素守恒计算分析;
解答 解:A、可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,在一定条件下,将2mol CO和1mol SO2充入一恒容密闭容器中,发生反应:SO2(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+S(l)△H=-akJ•mol-1,当达到平衡状态时生成二氧化碳一定小于2mol,故A错误;
B、反应焓变的意义是指反应物按照化学方程式计量数恰好全部反应放出的热量,反应是可逆反应,在一定条件下,将2mol CO和1mol SO2充入一恒容密闭容器中,不可能全部反应,反应放出热量小于aKJ,故B错误;
C、依据碳元素守恒分析判断,将2mol CO和1mol SO2充入一恒容密闭容器中,一氧化碳和二氧化碳总物质的量为2mol,故C正确;
D、结合氧元素守恒计算分析,将2mol CO和1mol SO2充入一恒容密闭容器中达到平衡状态,氧原子共4mol,故D错误;
故选C.
点评 本题考查了可逆反应达到平衡状态的特征分析判断,可逆反应不能进行程度,反应的焓变是指全部反应放出的热量,注意知识的积累,题目较简单.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
20.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L苯的分子数约为NA个 | |
| B. | 常温下,在1moLCnH2n+2中含有共价键数(3n+1)NA | |
| C. | 标准状况下,17g NH3所含共价键数为NA个 | |
| D. | 标准状况下,2.24L NO与1.12LO2混合后,所含分子数为0.2NA |
17.在2L的密闭容器内充人2moL N2和3mo1 H2,在一定的条件下使其反应,5min后测得反应混合物中NH3占25%(体积分数),则此时用N2表示的化学反应速率是( )
| A. | 0.05mol/(L•min ) | B. | 0.1mol/(L•min ) | C. | 0.125mol/(L•min ) | D. | 0.25mol/(L•min ) |
4.下列说法正确的是( )
| A. | Cl2的摩尔质量等于它的相对分子质量 | |
| B. | 1mol H2O的质量是18g | |
| C. | 氧气的摩尔质量是32g | |
| D. | 2g H2含1mol H |
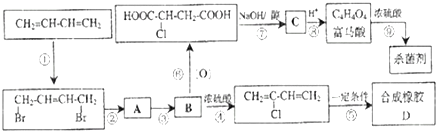

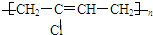
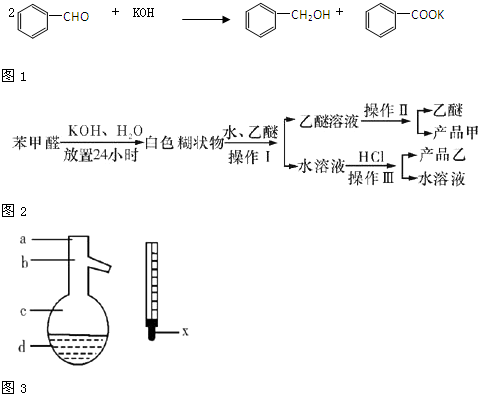

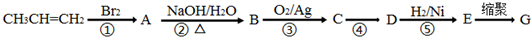
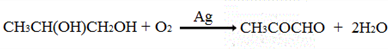 ;
;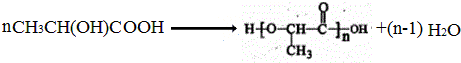 .
.