题目内容
有3个热化方程式:H2(g)+1/2O2(g)=H2O(g);△H ="a" kJ/mol
H2(g)+1/2O2(g)=H2O(l);△H =bkJ/mol
2H2(g)+O2(g)=2H2O(l);△H =ckJ/mol
关于它们的下列表述正确的是( )

H2(g)+1/2O2(g)=H2O(l);△H =bkJ/mol

2H2(g)+O2(g)=2H2O(l);△H =ckJ/mol

关于它们的下列表述正确的是( )

| A.a+b=c |
B.1mol H2O由气态变为液态吸收(a-b)kJ热量 |
C.氢气的燃烧热为c/2 kJ |
| D.1molH2 O由液态变为气态吸收l c/2-al kJ热量 |
D
本题考查反应热的计算。将2式减去1式可得,H2O(g)=H2O(l);△H =(b-a)kJ/mol,则B错误;H2O由气态变为液态是放出热量,所以b-a<0,即b<a,从热化方程式中计量数和物质的状态可知,2b=c,则A错误;燃烧热是正值,所以氢气的燃烧热为-c/2 kJ,C错误;D项正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
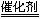 (3+2x)N2+6xH2O
(3+2x)N2+6xH2O