题目内容
【题目】下列有关化学用语使用正确的是
A. 次氯酸的结构式:H—Cl—O B. 乙醇的结构简式: C2H6O
C. 硫离子的结构示意图:![]() D. 丙烷分子的球棍模型:
D. 丙烷分子的球棍模型:![]()
【答案】D
【解析】A.次氯酸分子中不存在氢氯键,其中心原子为氧原子;B.乙醇的的结构简式中要标出官能团;C.硫离子与硫原子的核电荷数相同,所以硫离子的核电荷数应该为16,不是18;D、注意区分球棍模型和比例模型。
A.次氯酸的电子式为:![]() ,将电子式中所有共用电子对换成短线,即为次氯酸的结构式,所以次氯酸的结构式为:H-O-Cl,选项A错误;B.乙醇的结构简式为C2H5OH, C2H6O为乙醇的分子式,选项B错误;C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示意图为:
,将电子式中所有共用电子对换成短线,即为次氯酸的结构式,所以次氯酸的结构式为:H-O-Cl,选项A错误;B.乙醇的结构简式为C2H5OH, C2H6O为乙醇的分子式,选项B错误;C.硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示意图为: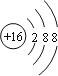 ,选项C错误;D、
,选项C错误;D、![]() 原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,选项D正确。答案选D。
原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,选项D正确。答案选D。

【题目】(1)氯化铵的水溶液显弱酸性,其原因为___________________(用离子方程式表示),0.1 molL-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度__________(填“增大”或“减小”);
(2)25℃,两种酸的电离平衡常数如下表。
化学式 | CH3COOH | H2CO3 | HCN | HClO | H2SO3 |
电离常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 5×10-10 | 3.0×10-8 | K1=2×10-2 K2=1×10-7 |
①物质的量浓度均为0.1 mol/L的四种溶液:
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由大到小的顺序为__________(用编号填写)。
②根据上表数据判断,下列离子方程式错误的是__________。
A.CO2(过量)+H2O+ClO-=HCO3-+HClO B.SO2(过量)+H2O+ClO-=HSO3-+HClO
C.CO2(少量)+H2O+CN-=HCO3-+HCN D.SO2(少量)+H2O+CN-=HSO3-+HCN
E.SO2(少量)+2CO32-+H2O=SO32-+2HCO3- F.2SO2(过量)+CO32-+H2O=2HSO3-+CO2↑
③0.10 molL-1Na2SO3溶液中离子浓度由大到小的顺序为___________________。
④25℃时,NaCN与HCN的混合溶液,若c(CN-)=c(HCN),则溶液中pH=__________(已知lg2=0.3,lg5=0.7)。
⑤25℃时,若向NaHSO3溶液中加入少量的I2,则溶液中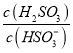 将__________(填“增大”“减小”或“不变”)。
将__________(填“增大”“减小”或“不变”)。