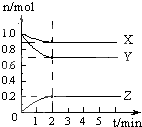题目内容
【题目】有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl)与c(SO42)之比为( ) 
A.1:1
B.2:3
C.3:2
D.2:1
【答案】B
【解析】解:设氢氧化钠物质的量浓度为1mol/L,首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为0.25V,物质的量为0.25Vmol,则n(Al3+)=0.25Vmol,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的物质的量为0.25Vmol×3=0.75Vmol,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液V,计算沉淀Mg2+消耗的氢氧化钠溶液的物质的量为Vmol﹣0.75molV=0.25Vmol,则n(Mg2+)=0.125Vmol,n(Cl﹣)=0.25Vmol;n(Al3+)=0.25Vmol,n(SO42﹣)= ![]() n(Al3+)=
n(Al3+)= ![]() ×0.25Vmol,溶液中c(Cl﹣):c(SO42﹣)=n(Cl﹣):n(SO42﹣)=0.25Vmol:
×0.25Vmol,溶液中c(Cl﹣):c(SO42﹣)=n(Cl﹣):n(SO42﹣)=0.25Vmol: ![]() ×0.25Vmol=2:3.
×0.25Vmol=2:3.
故选:B.
设氢氧化钠物质的量浓度为1mol/L,首先发生反应Mg2++2OH﹣═Mg(OH)2↓、Al3++3OH﹣═Al(OH)3↓,然后发生反应Al(OH)3+OH﹣═AlO2﹣+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为0.25V,物质的量为0.25Vmol,则n(Al3+)=0.25Vmol,根据离子方程式Al3++3OH﹣═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的物质的量为0.25Vmol×3=0.75Vmol,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液V,计算沉淀Mg2+消耗的氢氧化钠溶液的物质的量为Vmol﹣0.75molV=0.25Vmol,确定溶液中n(Mg2+)和n(Al3+),据此计算n(Cl﹣)与n(SO42)进行解答.

【题目】表是周期表中的一部分,根据A﹣I在周期表中的位置,第(1)~(3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答.
族 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)写出金属性最强元素与水的方应的方程式:
(2)A分别与D、E、G、形成的化合物中,稳定性由弱到强的顺序: ,
(3)F、H元素对应的最高价氧化物含氧酸由强到弱的顺序是: ,
(4)A和E组成化合物比A和F组成化合物的沸点(填“高”或“低”),原因是
(5)用电子式表示B的最高价氧化物对应的水化物的形成过程
(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式