题目内容
(14分)二氧化硫和氮的氧化物是重要的化工原料,同时也是造成大气污染的主要物质。对其性质的研究是化学的重要任务。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。根据图示回答下列问题:
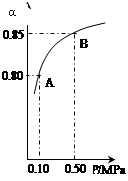
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)N2O5在四氯化碳溶液中的分解反应为:2N2O5=4NO2+O2。实验测得在67℃时反应体系中N2O5的物质的量浓度随时间的变化如下表所示。
①实验进行的前1分钟和最后1分钟,用N2O5的物质的量浓度变化表示的平均反应速率分别是 、 。
②实验进行的最后1分钟,用NO2的物质的量浓度变化表示的平均反应速率是 ;5分钟时NO2的物质的量浓度是 。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中放出的热量为____kJ。
(1)硫酸生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)
 2SO3(g)
2SO3(g)某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如右图所示。根据图示回答下列问题:

①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于_____。
②平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)N2O5在四氯化碳溶液中的分解反应为:2N2O5=4NO2+O2。实验测得在67℃时反应体系中N2O5的物质的量浓度随时间的变化如下表所示。
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c(N2O5)/mol·L—1 | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②实验进行的最后1分钟,用NO2的物质的量浓度变化表示的平均反应速率是 ;5分钟时NO2的物质的量浓度是 。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2,整个过程中放出的热量为____kJ。

略

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
 2C(g)若开始时只充入2molC(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molA和1molB的混合气体,达平衡时A的转化率为( )
2C(g)若开始时只充入2molC(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molA和1molB的混合气体,达平衡时A的转化率为( )  3C(g)+2D(g),达到平衡状态的是
3C(g)+2D(g),达到平衡状态的是 Z(g)+2W(g) △H<0,反应进行到5s时测得X的转化率为25%,10 s后达到化学平衡,测得Z的浓度为0.5mol/L,则下列说法正确的是
Z(g)+2W(g) △H<0,反应进行到5s时测得X的转化率为25%,10 s后达到化学平衡,测得Z的浓度为0.5mol/L,则下列说法正确的是 2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
2NO2(g)的压力平衡常数Kp分别为0.141和0.363。 2C(g) +2D(g),2 min 末反应达到平衡状态,生成0.8 mol D,请填写下面空白:
2C(g) +2D(g),2 min 末反应达到平衡状态,生成0.8 mol D,请填写下面空白: 2SO3(g) △H=―190 kJ·mol—1
2SO3(g) △H=―190 kJ·mol—1 的是_______________。(填字母)
的是_______________。(填字母)