题目内容
【题目】现有7种元素的性质如下表所示,它们位于第二或第三周期,下列判断错误的是( )

A.编号为⑥的元素比编号为②的元素金属性强,所以⑥的单质能从②形成的盐溶液中置换出②的单质
B.编号为④⑤的原子之间可形成共价化合物
C.编号为⑦的元素的最低价氢化物与最高价氧化物对应的水化物能反应生成盐
D.编号为⑥的单质一般保存在煤油中
【答案】A
【解析】
元素①化合价只有-2,①是O元素;元素⑤化合价为+7、-1,⑤是Cl元素;元素③⑥的化合价都是+1,且⑥的半径大于③,所以③是Li元素、⑥是Na元素;元素④⑦的化合价都是+5、-3,且④的半径大于⑦,所以④是P元素、⑦是N元素;②的化合价是+2,半径大于Li,所以②是Mg元素。
A.⑥是Na、②是Mg,Na元素金属性强比Mg强,由于Na能与水反应,所以Na不能从镁盐溶液中置换出Mg,故A错误;
B. ④是P元素、⑤是Cl元素,原子之间可形成共价化合物PCl3、PCl5,故B正确;
C. ⑦是N元素,最低价氢化物是NH3,最高价氧化物对应的水化物是HNO3,NH3、HNO3能反应生成NH4NO3,故C正确;
D. ⑥是Na元素,金属钠性质活泼,密度比煤油大,所以一般保存在煤油中,故D正确;
选A。

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
【题目】下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b﹤d。符合上述实验结果的盐溶液是
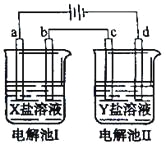
选项 | X | Y |
A. | MgSO4 | CuSO4 |
B. | AgNO3 | Pb(NO3)2 |
C. | FeSO4 | Al2(SO4)3 |
D. | CuSO4 | AgNO3 |