题目内容
14.舍勒在研究一种白色盐时发现,在黑暗中这种盐并无气味,而在光照条件下变黑,并产生一种刺激性气味(无液体).这种盐是( )| A. | AgBr | B. | AgI | C. | AgCl | D. | KClO3 |
分析 AgCl、KClO3为白色,AgBr为浅黄色,AgI为黄色,光照时,AgF难以分解,其它三种易分解,以此来解答.
解答 解:A.AgBr为浅黄色固体,光照条件下易分解,与题目不符,故A不选;
B.AgI为黄色固体,光照条件下易分解,与题目不符,故B不选;
C.AgCl为白色固体,光照条件下易分解,生成刺激性气体为氯气,故C选;
D.KClO3为白色固体,光照不分解,加热分解生成无色无味的气体氧气,故D不选;
故选C.
点评 本题考查卤化银的性质,为基础性习题,注意常见卤化银的颜色、水溶性以及稳定性的异同,题目难度不大.

练习册系列答案
相关题目
4.下列有关物质结构的表述正确的是( )
| A. | 次氯酸的电子式: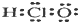 | B. | 氯化钠的分子式:NaCl | ||
| C. | 二氧化碳的比例模型: | D. | Cl-的结构示意图: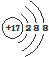 |
5.如图所示,锥形瓶内有气体X,分液漏斗内有液体Y,如果Y流下,过一会儿,小气球鼓起,气体X和Y不可能是( )


| A. | X是NH3,Y是KCl溶液 | B. | X是SO2,Y是NaOH | ||
| C. | X是H2,Y是浓硫酸 | D. | X是CO2,Y是KOH |
2.电解法炼铝时,冰晶石的作用是( )
| A. | 助熔剂 | B. | 催化剂 | C. | 还原剂 | D. | 氧化剂 |
9.氯碱工业在化工生产中占有十分重要的地位,电解前对饱和食盐水先要进行精致,以除去其中的泥沙、Ca2+、Mg2+、Fe3+、SO42-,其操作有:①加适量的盐酸②过量的BaCl2溶液③过量的Na2CO3溶液④过量的NaOH溶液⑤过滤.合理的操作步骤是( )
| A. | ①②③④⑤ | B. | ③②④⑤① | C. | ④②③⑤① | D. | ③④②⑤① |
19.下列钠的化合物及其性质或用途不相符的是( )
| A. | Na2O2-淡黄色固体,可用做漂白剂 | B. | Na2O-白色固体,性质不稳定 | ||
| C. | NaHCO3-受热易分解,可用做发酵粉 | D. | Na2CO3-性质稳定,可治疗胃酸过多 |
4.短周期元素的原子,处于基态时可能具有的电子是( )
| A. | 只有s和p电子 | B. | 只有s电子 | C. | 只有p电子 | D. | 有s、p和d电子 |