题目内容
下列表示对应反应的离子方程式正确的是
A.用惰性电极电解氯化镁溶液:2Cl-+2H+ H2↑+Cl2↑ H2↑+Cl2↑ |
| B.亚硫酸钠溶液中投入Na2O2: SO32-+2Na2O2=SO42-+O2↑+4Na+ |
| C.Fe2O3溶于足量的氢碘酸溶液中:Fe2O3+6H+=2Fe3++3H2O |
| D.鸡蛋壳和醋酸溶液的主要反应:CaCO3+2CH3COOH=2CH3COO-+Ca2++H2O+CO2↑ |
D
试题分析:氯离子和氢氧根离子移向阳极,氯离子容易失去电子,被氧化为氯气,镁离子和氢离子移向阴极,氢离子容易得到电子,被还原为氢气,由于氢离子是水电离出的,水是极弱电解质,应保留化学式,即2Cl-+2H2O
 2OH—+H2↑+Cl2↑,故A选项错误;观察可知,两边氧原子个数不守恒,硫元素和氧元素的化合价都升高,违反客观反应事实,根据电子、电荷、原子守恒原理配平可得:SO32—+Na2O2+H2O=SO42—+2Na++2OH—,故B选项错误;铁离子与碘离子容易发生氧化还原反应,生成亚铁离子和单质碘,则氧化铁溶于足量氢碘酸的反应为Fe2O3+6H++2I—=2Fe2++I2+3H2O,故C选项错误;鸡蛋壳的主要成分是碳酸钙,醋酸的酸性比乙酸强,因此鸡蛋壳与醋酸溶液易反应,生成醋酸钙溶液、水和二氧化碳气体,碳酸钙是难溶物、醋酸是弱酸、水是弱电解质、二氧化碳气体是非电解质,都应该保留化学式,醋酸钙是易溶的强电解质,应该改写成离子形式,故D选项正确。
2OH—+H2↑+Cl2↑,故A选项错误;观察可知,两边氧原子个数不守恒,硫元素和氧元素的化合价都升高,违反客观反应事实,根据电子、电荷、原子守恒原理配平可得:SO32—+Na2O2+H2O=SO42—+2Na++2OH—,故B选项错误;铁离子与碘离子容易发生氧化还原反应,生成亚铁离子和单质碘,则氧化铁溶于足量氢碘酸的反应为Fe2O3+6H++2I—=2Fe2++I2+3H2O,故C选项错误;鸡蛋壳的主要成分是碳酸钙,醋酸的酸性比乙酸强,因此鸡蛋壳与醋酸溶液易反应,生成醋酸钙溶液、水和二氧化碳气体,碳酸钙是难溶物、醋酸是弱酸、水是弱电解质、二氧化碳气体是非电解质,都应该保留化学式,醋酸钙是易溶的强电解质,应该改写成离子形式,故D选项正确。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 + CO2 +H2O→
+ CO2 +H2O→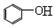 + HCO3-
+ HCO3-
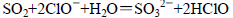


 NH3↑+H2O
NH3↑+H2O Cl2 ↑+H2 ↑+2OH—
Cl2 ↑+H2 ↑+2OH—