题目内容
【题目】80 ℃时,在2 L密闭容器中充入0.40 mol N2O4,发生反应N2O4(g) ![]() 2NO2(g) ΔH=+Q kJ·mol-1(Q>0),获得如下数据:
2NO2(g) ΔH=+Q kJ·mol-1(Q>0),获得如下数据:
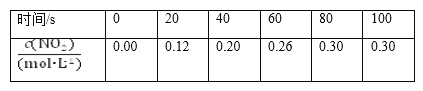
下列判断正确的是( )。
A.升高温度该反应的平衡常数K减小
B.20~40 s内,v(N2O4)=0.004 mol·L-1·s-1
C.反应达平衡时,吸收的热量为0.30Q kJ
D.100 s时再通入0.40 mol N2O4,达到新平衡时N2O4的转化率增大
【答案】C
【解析】
A.正反应为吸热反应,升高温度,平衡正向移动,平衡常数增大,故A错误;
B.20~40 s 内△v(NO2)=(0.2-0.12)mol/L=0.08mol/L,v(NO2)=![]() =0.004 molL-1s1,速率之比等于其化学计量数之比,则v(N2O4)=
=0.004 molL-1s1,速率之比等于其化学计量数之比,则v(N2O4)=![]() v(NO2)=0.002 molL-1s1,故B错误;
v(NO2)=0.002 molL-1s1,故B错误;
C.80s时到达平衡,生成二氧化氮为0.3mol/L×2L=0.6mol,由热化学方程式可知吸收的热量为QkJ×![]() =0.3QkJ,故C正确;
=0.3QkJ,故C正确;
D.100 s 时再通入0.40 mol N2O4,等效为在原平衡的基础上增大压强,与原平衡相比,平衡逆向移动,达新平衡时N2O4的转化率减小,故D错误;
故选C。

【题目】常温,下列实验操作及现象与推论不相符的是( )
选项 | 操作及现象 | 推论 |
A | 用pH试纸测得0.1mol/LCH3COOH溶液pH约为3 | CH3COOH是弱电解质 |
B | 向某无色溶液中加入足量稀盐酸,产生无色无味气体;再将该气体通入澄清石灰水,产生白色浑浊 | 溶液中可能含有CO |
C | 用pH计测定相同浓度的CH3COONa溶液和NaClO溶液的pH,前者的pH小于后者的 | HClO的酸性弱于CH3COOH |
D | 向2mL1mol/LNaOH溶液中加入1mL0.1mol/LMgCl2溶液,产生白色沉淀;再加入1mL0.1mol/LFeCl3溶液,产生红褐色沉淀 | Mg(OH)2沉淀转化为Fe(OH)3沉淀 |
A.AB.BC.CD.D
【题目】判断正误(在答题卡表格中①~题题号对应位置画“√”或“×”)。
(1)2020年6月23日9时43分北斗系统第五十五颗导航卫星暨北斗三号最后一颗全球组网卫星成功发射!执行本次发射任务的长三乙运载火箭加装的常规燃料为偏二甲肼(C2H8N2)和四氧化二氮。偏二甲肼和四氧化二氮也可以作为燃料电池的两极反应物。二者反应的产物均对环境不产生污染。根据以上信息判断下列说法正误:
①偏二甲肼是有机物,其中氮元素化合价为-3_____
②生成1molCO2转移8mol电子_____
③偏二甲肼与四氧化二氮的反应是放热反应_____
④该燃料电池中偏二甲肼是负极反应物_____
(2)如图所示装置,用生成的氯气与乙二醛制备乙二酸,反应原理为![]() +2Cl2+2H2O→
+2Cl2+2H2O→![]() +4HCl。
+4HCl。
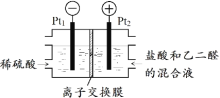
判断以下说法的正误:
⑤该装置利用上述反应将电能全部转化为化学能_____
⑥Pt1电极的反应式为2H2O+2e-=H2↑+2OH-_____
⑦盐酸除增强溶液导电性的作用,还提供Cl-参与电极反应_____
⑧理论上每得到0.1mol乙二酸,将有0.4molH+从右室迁移到左室_____
(3)判断对下列图像的描述的正误:
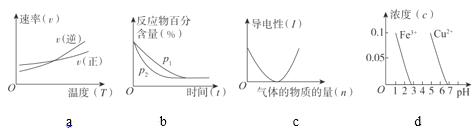
⑨根据图a可判断反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0_____
2AB3(g)的ΔH>0_____
⑩图b可表示压强(P)对反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响_____
3C(g)+D(s)的影响_____
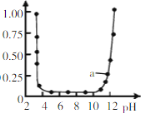
图c可表示向醋酸溶液通入氨气时,溶液导电性随氨气量的变化_____
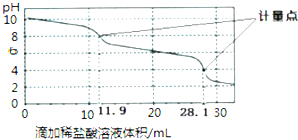
根据图d,除去CuSO4溶液中的Fe3+,可加入NaOH调节pH至3~4_____
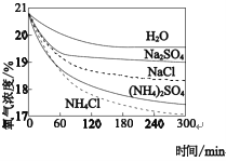
(4)利用如下实验探究铁钉在不同溶液中的吸氧腐蚀。
实验装置 | 实验编号 | 浸泡液 | pH | 氧气浓度随时间的变化 |
| i | H2O | 7 |
|
ii | 1.0mol·L-1NH4Cl | 5 | ||
iii | 0.5mol·L11(NHspan>4)2SO4 | 5 | ||
iv | 1.0mol·L-1NaCl | 7 | ||
v | 0.5mol·L-1Na2SO4 | 7 |
通过以上实验判断下列说法正误:
i与iv、v比较说明盐溶液可以加快吸氧腐蚀速率_____
ii与iii、iv与v比较说明吸氧腐蚀速率与阴离子种类无关_____
向实验v溶液中加入少量(NH4)2SO4固体,吸氧腐蚀速率加快_____
向实验ii溶液中加等体积的0.5mol·L-1(NH4)2SO4,吸氧腐蚀速率一定加快_____