题目内容
【题目】碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱。
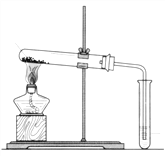
(1)用上图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是_________。通过本实验证明,这两种固体对热的稳定性是Na2CO3 ________于(选填“强”或“弱”)NaHCO3。
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能观察到的现象是__________________,其中碳酸氢钠和稀盐酸反应的化学方程式为_______________________________。
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有 _________ 、_________ 等。
【答案】 碳酸氢钠(NaHCO3) 强 产生气泡 NaHCO3 + HCl =NaCl+ H2O + CO2↑ NaNO3 Na2SO4
【解析】(1)NaHCO3受热易分解,Na2CO3受热不分解,碳酸钠较碳酸氢钠稳定,则观察到澄清石灰水变浑浊时,则试管中加热的固体是NaHCO3,故答案为:NaHCO3;强;
(2)二者均与盐酸反应生成二氧化碳,观察到的现象为有气泡冒出,碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,其化学反应为NaHCO3+HCl=NaCl+H2O+CO2↑,故答案为:有气泡冒出;NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)氧化钠、氯化钠、过氧化钠、硫酸钠等均为常见的钠的化合物,故答案为:氧化钠;氯化钠;NaNO3;Na2SO4(任选2个即可)

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目