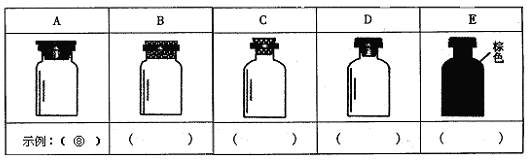
��Ŀ����
��Ҫ����գ�
��1�������Ԫ��ԭ�Ӱ뾶��С����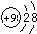
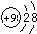 ��
��
��2��Ϊ��ֹ̼�ظֲ˵����⣬ʹ�ú��ر����й��̲˺�Ӧ��ȡ�ļ��״�ʩ��
��3����Է�������Ϊ58�������ķ���ʽ��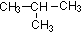
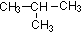
��4����֪ij��Ӧ�ĸ�����Ũ���������£�aA��g��+bB��g�� 2C��g��
2C��g��
��ʼŨ�ȣ�mol/L����1.5 1.0 0
2sĩŨ�ȣ�mol/L����0.9 0.8 0.4
���a=
��2S��B�ķ�Ӧ����=
��3sĩ������Ӧ��ƽ��ʱ��CŨ��Ϊ0.6mol/L����A��ת����Ϊ
��5����6�֣���ϩͨ����ˮ����ɫ�Ļ�ѧ����ʽ��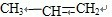 +Br2��
+Br2��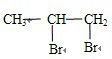
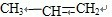 +Br2��
+Br2�� ����Ӧ���ͣ�
����Ӧ���ͣ�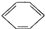 +HO-NO2
+HO-NO2
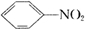 +H2O
+H2O +HO-NO2
+HO-NO2
 +H2O����Ӧ���ͣ�
+H2O����Ӧ���ͣ�
��1�������Ԫ��ԭ�Ӱ뾶��С����
�
�
������Ϊ��һ����ɫ�ɳ��صIJ��ϣ��ŵ�ʱ���ǵ�ص���
��
�����������������±��Ԫ����ԭ�������ĵ���������7
7
�����ڻ�ѧ��Ӧ���������õ�1
1
�����ӣ���±��Ԫ���зǽ�������ǿ��Ԫ������
��
�������ӵĽṹʾ��ͼ��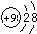
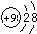
��2��Ϊ��ֹ̼�ظֲ˵����⣬ʹ�ú��ر����й��̲˺�Ӧ��ȡ�ļ��״�ʩ��
�������˵����øɾ�
�������˵����øɾ�
�� �����к���������õ�ȼ������������ҪԪ����C��H
C��H
��������ȼ�պ����ɵĻ�������Ҫ��CO2��H2O
CO2��H2O
����3����Է�������Ϊ58�������ķ���ʽ��
C4H10
C4H10
�������ܵĽṹ��ʽ��CH3-CH2-CH2-CH3
CH3-CH2-CH2-CH3
��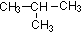
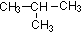
��4����֪ij��Ӧ�ĸ�����Ũ���������£�aA��g��+bB��g��
 2C��g��
2C��g����ʼŨ�ȣ�mol/L����1.5 1.0 0
2sĩŨ�ȣ�mol/L����0.9 0.8 0.4
���a=
3
3
��b1
1
����2S��B�ķ�Ӧ����=
0.1mol/��L?S��
0.1mol/��L?S��
����3sĩ������Ӧ��ƽ��ʱ��CŨ��Ϊ0.6mol/L����A��ת����Ϊ
60%
60%
����5����6�֣���ϩͨ����ˮ����ɫ�Ļ�ѧ����ʽ��
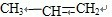 +Br2��
+Br2��
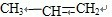 +Br2��
+Br2��
�ӳɷ�Ӧ
�ӳɷ�Ӧ
�����������ɵĻ�ѧ����ʽ�� +HO-NO2
+HO-NO2
| ||
| �� |
 +H2O
+H2O +HO-NO2
+HO-NO2
| ||
| �� |
 +H2O
+H2Oȡ����Ӧ
ȡ����Ӧ
����������1��ͬһ����Ԫ�ص�ԭ�ӣ����ϵ���ԭ�Ӱ뾶�����ǽ�����������ԭ����У����ý������������ڢ���AԪ�س�Ϊ±��Ԫ�أ�������������7��
��2���������ԭ���ǽ�������ˮ�������Ӵ�����������õ�ȼ������Ȼ����ȼ�ղ�����ˮ�Ͷ�����̼��
��3����������ͨʽ��CnH2n+2������������ͬ���칹�壻
��4���ٻ�ѧ��Ӧ�и������ʵ�Ũ�ȵı仯��֮�ȵ��ڷ���ʽ��ϵ��֮�ȣ�
�ڸ���v=
�����㷴Ӧ���ʣ�
�۸���A��ת����=
��100%�����㣻
��5����ˮ�ͱ�ϩ֮�䷢���ӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ������������
��2���������ԭ���ǽ�������ˮ�������Ӵ�����������õ�ȼ������Ȼ����ȼ�ղ�����ˮ�Ͷ�����̼��
��3����������ͨʽ��CnH2n+2������������ͬ���칹�壻
��4���ٻ�ѧ��Ӧ�и������ʵ�Ũ�ȵı仯��֮�ȵ��ڷ���ʽ��ϵ��֮�ȣ�
�ڸ���v=
| ��c |
| t |
�۸���A��ת����=
| A��Ũ�Ȼ����ʵ����ı仯�� |
| ��ʼŨ�Ȼ�仯�� |
��5����ˮ�ͱ�ϩ֮�䷢���ӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ������������
����⣺��1�������Ԫ�ص�ԭ�ӣ����ϵ���ԭ�Ӱ뾶������ԭ�Ӱ뾶��С���ǽ���ﮣ�﮵�طŵ�ʱ����ǵ�صĸ�����±��Ԫ�ص�ԭ�ӣ����ϵ��·ǽ��������������Էǽ�������ǿ��Ԫ����F���ڢ���AԪ�س�Ϊ±��Ԫ�أ�������������7�ڻ�ѧ��Ӧ���������õ�1�����ӣ��γ�8�����ȶ��ṹ���ʴ�Ϊ��ﮣ�����7��1������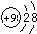 ��
��
��2���������ԭ���ǽ�������ˮ�������Ӵ����й��̲˺�IJ˵�����ֹ����ļ������ǣ��������˵����øɾ�����������õ�ȼ������Ȼ����ȼ�ղ�����ˮ�Ͷ�����̼���ʴ�Ϊ���������˵����øɾ���C��H��CO2��H2O��
��3����������ͨʽ��CnH2n+2����Է�������Ϊ14n+2������Է�������Ϊ58ʱ������n=4����Ϊ���飬����2��ͬ���칹�壺��������춡�飬�ʴ�Ϊ��C4H10��CH3-CH2-CH2-CH3��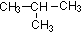 ��
��
��4����A��B��Ũ�ȵı仯���ֱ�Ϊ��0.6mol/L��0.2mol/L��Ũ�ȵı仯��֮�ȵ��ڷ���ʽ��ϵ��֮�ȣ�����a=3��b=1���ʴ�Ϊ��3��1��
��2S��B�ķ�Ӧ����v=
=
=0.1mol/��L?S�����ʴ�Ϊ��0.1mol/��L?S����
��3sĩ������Ӧ��ƽ��ʱ��CŨ��Ϊ0.6mol/L�������ĵ�A��Ũ��Ϊ0.9mol/L��A��ת����=
��100%=
��100%=60%���ʴ�Ϊ��60%��
��5����ˮ�ͱ�ϩ֮�䷢���ӳɷ�Ӧ��ԭ���ǣ�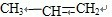 +Br2��
+Br2�� �����ڼӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ��������������
�����ڼӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ�������������� +HO-NO2
+HO-NO2
 +H2O������ȡ����Ӧ���ʴ�Ϊ��
+H2O������ȡ����Ӧ���ʴ�Ϊ��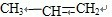 +Br2��
+Br2�� ���ӳɷ�Ӧ��
���ӳɷ�Ӧ�� +HO-NO2
+HO-NO2
 +H2O��ȡ����Ӧ��
+H2O��ȡ����Ӧ��
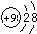 ��
����2���������ԭ���ǽ�������ˮ�������Ӵ����й��̲˺�IJ˵�����ֹ����ļ������ǣ��������˵����øɾ�����������õ�ȼ������Ȼ����ȼ�ղ�����ˮ�Ͷ�����̼���ʴ�Ϊ���������˵����øɾ���C��H��CO2��H2O��
��3����������ͨʽ��CnH2n+2����Է�������Ϊ14n+2������Է�������Ϊ58ʱ������n=4����Ϊ���飬����2��ͬ���칹�壺��������춡�飬�ʴ�Ϊ��C4H10��CH3-CH2-CH2-CH3��
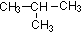 ��
����4����A��B��Ũ�ȵı仯���ֱ�Ϊ��0.6mol/L��0.2mol/L��Ũ�ȵı仯��֮�ȵ��ڷ���ʽ��ϵ��֮�ȣ�����a=3��b=1���ʴ�Ϊ��3��1��
��2S��B�ķ�Ӧ����v=
| ��c |
| t |
| 1.0mol/L-0.8mol/L |
| 2s |
��3sĩ������Ӧ��ƽ��ʱ��CŨ��Ϊ0.6mol/L�������ĵ�A��Ũ��Ϊ0.9mol/L��A��ת����=
| A��Ũ�Ȼ����ʵ����ı仯�� |
| ��ʼŨ�Ȼ�仯�� |
| 0.9mol/L |
| 1.5mol/L |
��5����ˮ�ͱ�ϩ֮�䷢���ӳɷ�Ӧ��ԭ���ǣ�
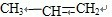 +Br2��
+Br2�� �����ڼӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ��������������
�����ڼӳɷ�Ӧ������Ũ�����Լ�Ũ����Ļ���ᷴӦ�������������� +HO-NO2
+HO-NO2
| ||
| �� |
 +H2O������ȡ����Ӧ���ʴ�Ϊ��
+H2O������ȡ����Ӧ���ʴ�Ϊ��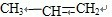 +Br2��
+Br2�� ���ӳɷ�Ӧ��
���ӳɷ�Ӧ�� +HO-NO2
+HO-NO2
| ||
| �� |
 +H2O��ȡ����Ӧ��
+H2O��ȡ����Ӧ��������������һ���ۺ�֪ʶ��Ŀ������Ƕȹ㣬���Ը�����ѧ֪ʶ���лش��ѶȲ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ