��Ŀ����
��ijһ�ݻ�Ϊ5 L ���ܱ������ڣ����� 0.2 mol��CO��0.2 mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)+H2O(g)
���ܱ������ڣ����� 0.2 mol��CO��0.2 mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)+H2O(g) CO2(g)+H2(g)����H��0��Ӧ��CO2��Ũ����ʱ��仯�����
CO2(g)+H2(g)����H��0��Ӧ��CO2��Ũ����ʱ��仯����� ��ͼ��
��ͼ��
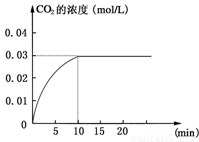
(1)������ͼ���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊv(CO)�� mol/(L��min)����Ӧ��ƽ��ʱ��c(H2)��____________mol/L�����¶��µ�ƽ�ⳣ��K= (��������)��
(2)�жϸ÷�Ӧ�ﵽƽ���������________________��
�� CO���ٵĻ�ѧ��Ӧ���ʺ�CO2���ٵĻ�ѧ��Ӧ�������
�� CO��H 2O��CO2��H2��Ũ�ȶ����
2O��CO2��H2��Ũ�ȶ����
�� CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
�� �����淴Ӧ���ʶ�Ϊ��
(3)��Ҫһ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.1 mol�� CO2��0.1 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c(H2O)��_____________mol/L��
 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д������£�������������Һ��
�� | �� | �� | �� |
0.1 mol/L NaOH��Һ | pH = 11 NaOH��Һ | 0.1 mol/L CH3COOH��Һ | pH = 3CH3COOH��Һ |
����˵����ȷ����(  )
)
A����ˮ�����H+��Ũ��c(H+)���٣���
B�����ܼ�����ˮϡ����ԭ����100��ʱ��������Һ��pH>5
C������ۻ�ϣ�����ҺpH=7���������V(NaOH)��V(CH3COOH)
D���������pH�Ģ���Һ������ֱ���������Zn��Ӧ������Һ����ͬ���������������
4���������������Ԫ�ص����λ�����,Ԫ��x��ԭ�Ӻ����������m��2��,y��������������ԡ�
|
| m | n |
x | y |
|
|
�ش���������:
��1��Ԫ��x�����ڱ��е�λ���� ,�䵥�ʿɲ��õ������ �ķ����Ʊ���
��2��������ӣ�mn��2�ĵ���ʽΪ ,��mn��2��Ϊ��±��,������±������,��������������Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��3����֪�軯�ƣ�NaCN��,������ܶ�����γ������,��˹�ҵ�ϲ����軯����������ϡ���軯����Һ���������˵Ľ��ʯ,ͨ�����,ʹ���ʯ�еĽ����ܽ�,����������ˮ�������Na[Au��CN��2],�䷴Ӧ����ʽΪ:��4Au+8NaCN+2H2O+O2=4Na[Au��CN��2]+4NaOH��Na[Au��CN��2]��ˮ��Һ�еĵ��뷽��ʽΪ:��Na[Au��CN��2]=Na++[Au��CN��2]-��Ȼ������п����Һ�аѽ��û�����,пת��ΪNa2[Zn��CN��4]���ݴˣ������â�д���ڿ��������軯����Һ��ȡ��ĵ缫��Ӧʽ:����: ������: ��
��4�����˲����軯���ж�,����Na2S2O3����,���߷�Ӧ�õ����ֺ���Ԫ�ص�����,����һ������Fe3+�ɱ�Ϊ��ɫ��д���ⶾԭ����������ӷ���ʽ ��


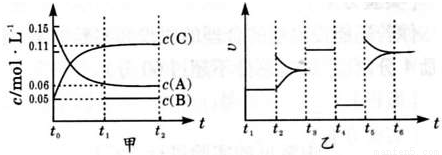
 B��g��+2C��g����H=-50akJ•mol-1
B��g��+2C��g����H=-50akJ•mol-1 ��
�� CO2(g)+2H2(g)
CO2(g)+2H2(g)

 ����ɫ�����й��ڸ���Һ���ж���ȷ����
����ɫ�����й��ڸ���Һ���ж���ȷ����
 �� ��
�� ��