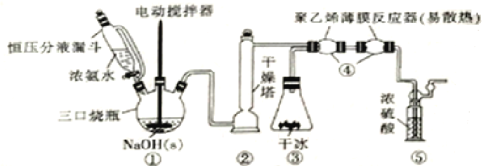
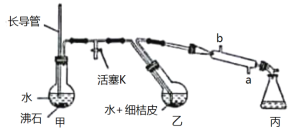
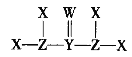题目内容
【题目】已知常温下HF酸性强于HCN,分别向1Ll mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积变化),溶液中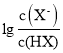 (X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
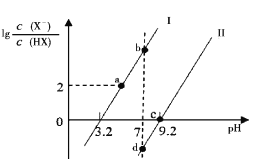
A.直线I对应的是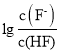
B.I中a点到b点的过程中水的电离程度逐渐增大
C.c点溶液中:![]()
![]()
D.b点溶液和d点溶液相比:cb(Na+)<cd(Na+)
【答案】D
【解析】
A.纵坐标为0时即![]() =1,此时Ka=
=1,此时Ka=![]() =c(H+),因此直线I对应的Ka=10-3.2, 直线II对应的Ka= 10-9.2, 由于HF酸性强于HCN,因此直线I对应
=c(H+),因此直线I对应的Ka=10-3.2, 直线II对应的Ka= 10-9.2, 由于HF酸性强于HCN,因此直线I对应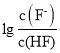 ,A正确;
,A正确;
B.a点到b点的过程中HF浓度逐渐减小,NaF浓度逐渐增大,因此水的电离程度逐渐增大,B正确;
C.Ka(HCN)= 10-9.2 ,NaCN的水解常数Kh(NaCN)=10-4.8>Ka(HCN),因此等浓度的HCN和NaCN的混合溶液中c(CN-)<c(HCN),c点是HCN和NaCN的混合溶液且c(CN-)=c(HCN),因此c(NaCN)>c(HCN),即有c(Na+)>c(CN-);由于OH-、H+来自水的电离,浓度比较小且此时溶液的pH为9.2,C点溶液中存在:c(Na+)>c(CN-)=c(HCN) >c(OH-)>c(H+),C正确;
D.由于HF酸性强于HCN,要使溶液均显中性,HF溶液中要加入较多的NaOH,因此cb(Na+)>cd(Na+),D错误;
答案选D。

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目