题目内容
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水.得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的分子量(相对分子质量)为( )
A. | B.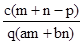 |
C. | D. |
C
首先求蒸发掉Pg水后溶质质量分数为: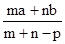 ,据物质的量浓度计算公式:物质的量浓度=
,据物质的量浓度计算公式:物质的量浓度=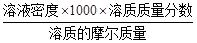 得:溶质的摩尔质量=
得:溶质的摩尔质量=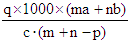 ,故答案C正确,答案选C。
,故答案C正确,答案选C。
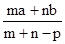 ,据物质的量浓度计算公式:物质的量浓度=
,据物质的量浓度计算公式:物质的量浓度=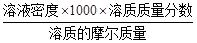 得:溶质的摩尔质量=
得:溶质的摩尔质量=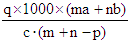 ,故答案C正确,答案选C。
,故答案C正确,答案选C。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 mol/L
mol/L mol/L
mol/L mol/L
mol/L mol/L
mol/L