题目内容
(1)1 mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2 L(标准状况)氢气,则A分子中必有一个 基,若此基在碳链的一端,且A中无支链,则A的结构简式为 。
(2)A与浓硫酸共热,分子内脱去1分子水,生成B,B的结构简式为 ;B通入溴水中能发生 反应,生成C,C的结构简式为 。
(3)A在铜作催化剂时,与氧气在加热条件下发生氧化还原反应生成D,D的结构简式为 。
写出下列指定反应的化学方程式:
①A→B ;
②B→C ;
③A→D 。
(1)羟;CH3CH2CH2OH
(2)CH3—CH—CH2;加成;CH3CHBr—CH2Br
(3)CH3CH2CHO
①CH3CH2CH2OH CH3CH—CH2↑+H2O
CH3CH—CH2↑+H2O
②CH3CH—CH2+Br2―→CH3CHBr—CH2Br
③2CH3CH2CH2OH+O2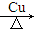 2CH3CH2CHO+2H2O
2CH3CH2CHO+2H2O
解析

 初中暑期衔接系列答案
初中暑期衔接系列答案(14分)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用下图A装置制备乙酸乙酯.
(1)若实验中用乙酸和含18O的乙醇作用,该反应的化学方程式是:
与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是 .
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层的厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL18mol?L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol?L-1H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.
(3)若现有乙酸90g,乙醇138g发生酯化反应得到88g乙酸乙酯,试计算该反应的产率为 .
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图.图中( )内为适当的试剂,【 】内为适当的分离方法.

①试剂a是 ;分离方法②是 ,分离方法③是 .分离方法①是分液,在具体操作中应充分振荡,然后静置,待分层后 (填标号),
A.直接将乙酸乙酯从分液漏斗上口倒出
B.直接将乙酸乙酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸乙酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出
②在得到的A中加入无水碳酸钠粉末,振荡,目的是 .
(5)为充分利用反应物,甲、乙两位同学分别设计了上面图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为最合理的是
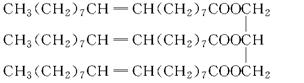



 最难。
最难。

