题目内容
【题目】20℃时,用0.1mol/L盐酸滴定20mL0.1mol/L氨水的图像如图所示,下列说法正确的是
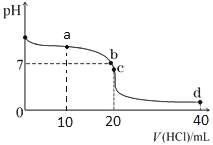
A.a点时2c(Cl-)=c(NH3H2O)+c(NH4+)
B.b点表示酸碱恰好完全反应
C.c点时c(NH4+)>c(Cl-)>c(H+)>c(OH-)
D.a、b、c、d均有c(NH4+)+c(H+)=c(Cl-)+c(OH-)
【答案】AD
【解析】
A. a点加入10mL的盐酸,溶液为等物质的量的氨水、氯化铵,根据物料守恒,则2c(Cl-)=c(NH3H2O)+c(NH4+),A项正确;
B. 20mL0.1mol/L氨水恰好完全反应需要0.1mol/L盐酸20mL,B项错误;
C. c点为氯化铵溶液显酸性,离子浓度大小关系为c(Cl-)>c(NH4+)> c(H+)>c(OH-),C项错误;
D. a、b点为氨水、氯化铵,c点为氯化铵,d点为盐酸、氯化铵,根据电荷守恒均有c(NH4+)+c(H+)=c(Cl-)+c(OH-),D项正确;
答案选AD。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】苯乙烯(![]() )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
![]() (g)
(g)![]()
![]() (g)+H2(g) △H
(g)+H2(g) △H
(1)已知:
化学键 | C-H | C-C | C=C | H-H |
键能/kJ/mol | 412 | 348 | 612 | 436 |
计算上述反应的△H=________ kJ·mol-1。
(2)500℃时,在恒容密闭容器中,充入a mol乙苯,反应达到平衡后容器内气体的压强为P;若再充入bmol的乙苯,重新达到平衡后容器内气体的压强为2P,则a_______b(填“>” “<”或“=”),乙苯的转化率将________(填“增大” “减小”或“不变”)。
(3)工业上,通常在乙苯(EB)蒸气中掺混N2(原料气中乙苯和N2的物质的量之比为1︰10,N2不参与反应),控制反应温度600℃,并保持体系总压为0.1Mpa不变的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
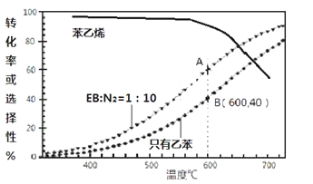
①A,B两点对应的正反应速率较大的是________。
②掺入N2能提高乙苯的平衡转化率,解释说明该事实___________________________。
③用平衡分压代替平衡浓度计算600℃时的平衡常数Kp=________。(保留两位有效数字,分压=总压×物质的量分数)
④控制反应温度为600℃的理由是___________________________。