题目内容
【题目】25℃时有甲、乙、丙三种溶液,甲为0.1mol·L-1NaOH溶液,乙为0.1mol·L-1HCl溶液,丙为0.1 mol·L-1CH3COOH溶液,请回答下列问题:
(1)甲溶液的pH=___________________。
(2)乙溶液中由水电离出的c(H+)=___________________mol·L-1。
(3)写出丙的电离方程式_________________________________________________________,其电离平衡常数表达式Ka=___________________。
(4)向丙中加入乙,会_____________(“抑制”或“促进”)丙的电离,c(H+)_____________(填“增大”、“减小”或“不变”), 丙的电离平衡常数Ka_____________(填“增大”、“减小”或“不变”)。
(5)各取25 mL的乙、丙两溶液,分别用甲中和至pH=7,则消耗甲的体积大小关系为V(乙) ____________V (丙)(填“大于”、“小于”或“等于”)。
【答案】13 1×10-13 CH3COOH ![]() H++CH3COO- c(H+) c(CH3COO-)/c(CH3COOH) 或
H++CH3COO- c(H+) c(CH3COO-)/c(CH3COOH) 或![]() 抑制 增大 不变 大于
抑制 增大 不变 大于
【解析】
(1)根据pH=-lgc(H+)计算;
(2)盐酸抑制水电离,由水电离出的c(H+)=溶液中的c(OH-);
(3)醋酸是弱电解质,部分电离为氢离子和醋酸根离子;根据电离平衡常数的定义书写表达式;
(4)0.1mol·L-1HCl溶液中氢离子浓度大于0.1 mol·L-1CH3COOH;电离平衡常数只与温度有关;
(5)NaCl是强酸强碱盐,其水溶液呈中性,醋酸钠是强碱弱酸盐,其水溶液呈碱性。
(1)0.1mol·L-1NaOH溶液中c(OH-)=0.1mol/L,c(H+)=Kw/ c(OH-)=1×10-13 mol/L, pH=-lgc(H+)=13;
(2)0.1mol·L-1HCl溶液中c(H+)=0.1mol/L、c(OH-)=1×10-13 mol/L,盐酸抑制水电离,所以由水电离出的c(H+)=溶液中的c(OH-)=1×10-13;
(3)醋酸是弱电解质,部分电离为氢离子和醋酸根离子,电离方程式是CH3COOH ![]() H++CH3COO-;其电离平衡常数表达式Ka=c(H+) c(CH3COO-)/c(CH3COOH);
H++CH3COO-;其电离平衡常数表达式Ka=c(H+) c(CH3COO-)/c(CH3COOH);
(4)0.1mol·L-1HCl溶液中氢离子浓度大于0.1 mol·L-1CH3COOH,向醋酸溶液中加入盐酸,c(H+)增大,CH3COOH ![]() H++CH3COO-逆向移动,所以抑制醋酸的电离;电离平衡常数只与温度有关,所以醋酸的电离平衡常数Ka不变;
H++CH3COO-逆向移动,所以抑制醋酸的电离;电离平衡常数只与温度有关,所以醋酸的电离平衡常数Ka不变;
(5)各取25 mL的乙、丙两溶液,加入氢氧化钠溶液,恰好完全反应时消耗氢氧化钠的体积相同,此时溶质分别是NaCl、醋酸钠,NaCl是强酸强碱盐,其水溶液呈中性,醋酸钠是强碱弱酸盐,其水溶液呈碱性,要使醋酸钠溶液呈中性,醋酸应该稍微多些,所以各取25mL的乙、丙两溶液,分别用氢氧化钠中和至pH=7,则消耗氢氧化钠的体积大小关系为V(乙)>V(丙);

 名校课堂系列答案
名校课堂系列答案【题目】I. 科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示部分(条件及物质未标出)。
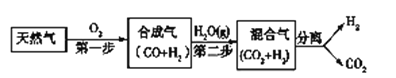
(1)工业上可用H2和CO2制备甲醇,其反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)+H2O(g),某温度下,将1 mol CO2和3 mol H2充入体积不变的2 L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
P后/P前 | 0.9 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
用H2 表示前2 h平均反应速率v(H2) =__________ mol·(L·h)-1。
(2)在300 ℃、8 MPa下,将二氧化碳和氢气按物质的量之比为1∶3通入一密闭容器中发生(1)中反应,达到平衡时,测得二氧化碳的平衡转化率为50%,则该反应条件下的平衡常数Kp= ________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)CO2经催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系:
C2H4(g)+4H2O(g) ΔH。在0.1 MPa时,按n(CO2)∶n(H2)=1∶3投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系:
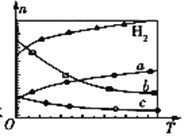
①该反应的ΔH ______ 0 (填“>”、“=”或“<”)。
②曲线c表示的物质为 ____________________。
II. 砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。某小组欲探究可逆反应AsO33-+I2+2OH- ![]() AsO43- + 2I- + H2O。设计如下图I所示装置。实验操作及现象:按图I装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图I装置左边烧杯中逐滴加入一定量2mol/L的盐酸,发现又产生电流,实验中电流与时的关系如图II所示。
AsO43- + 2I- + H2O。设计如下图I所示装置。实验操作及现象:按图I装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图I装置左边烧杯中逐滴加入一定量2mol/L的盐酸,发现又产生电流,实验中电流与时的关系如图II所示。
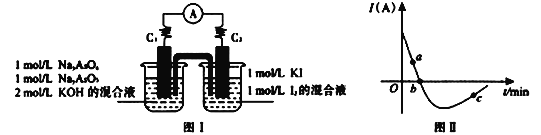
(1)图II中AsO43-的逆反应速率:a____b( 填“>”、“<”或“=” )。
(2)写出图II中c点对应图I装置的正极反应式__________________________。
(3)能判断该反应达到平衡状态的是________。
a.2v(I-)正=v(AsO33-)逆b.溶液的pH不再变化
c.电流表示数变为零 d.溶液颜色不再变化
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2。假设常温下在恒容的密闭容器中发生上述反应,试解答下列问题:
2CO2+N2。假设常温下在恒容的密闭容器中发生上述反应,试解答下列问题:
(1)上述条件下该反应能够自发进行,则反应的ΔH_____0(填写“>”、“<”、“=”)。
(2)能判断该反应达到化学平衡状态的依据是____________。
A.混合气体的压强保持不变
B.N2的浓度不再改变
C.消耗CO的物质的量与生成CO2的物质的量之比为1∶1
D.NO、CO、CO2、N2的物质的量之比为2∶2∶2∶1
(3)既要加快反应速率又要提高NO转化率,下列措施可行的是____________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)为了测定在某种催化剂作用下的反应速率,某科学家在某温度下用气体传感器测得不同时间的NO和CO浓度如表(均不考虑温度变化对催化剂催化效率的影响):
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) ( molL-1) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO) ( molL-1) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | X | 2.70×10-3 |
从表中数据分析可知:
①X=____________mol·L-1;
②前2s内的平均反应速率v(N2)=________________________mol·L-1·s-1;
③该温度下反应的平衡常数K=________________________。
