题目内容
(7分)实验室用20 g软锰矿(主要成分MnO2)与200 mL 12 mol/L的浓盐酸(足量)反应,制得标准状况下4.48L Cl2。过滤反应后的混合物得滤液,向滤液中加入足量的硝酸银溶液,产生白色沉淀。若浓盐酸的挥发忽略不计,试计算:
(1)软锰矿中MnO2的质量分数是多少?
(2)反应中被氧化的HCl物质的量为多少?
(3)滤液中加入足量硝酸银后产生的白色沉淀的质量是多少?
(1)软锰矿中MnO2的质量分数是多少?
(2)反应中被氧化的HCl物质的量为多少?
(3)滤液中加入足量硝酸银后产生的白色沉淀的质量是多少?
⑴87% ⑵0.4mol ⑶287g
试题分析: MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O1 4 1 1
xmol ymol zmol
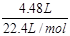
计算可知:x=0.2mol y=0.8mol z=0.2mol
MnO2的质量分数=
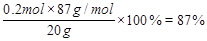
被氧化的HCl是参加反应的HCl的一半,所以被氧化的HCl为0.4mol
溶液中有n(Cl-)=0.4mol,所以产生氯化银的质量为0.4mol×143.5g/mol=287g
答:略
点评:本题是典型的通过物质的量计算的习题,对提高学生的计算水平有很大帮助。尤其近几年高考中化学已经出现书写计算过程的考题了,对于书写计算过程更应该注重步骤的完整。

练习册系列答案
相关题目