题目内容
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
(1)写出该反应的反应方程式:
3Fe+4H2O(g)
Fe3O4+4H2↑
| ||
3Fe+4H2O(g)
Fe3O4+4H2↑
;并指明该氧化还原反应的还原剂是
| ||
Fe
Fe
,氧化剂是H2O
H2O
.(2)烧瓶底部放置了几片碎瓷片,碎瓷片作用是
防止暴沸
防止暴沸
.(3)干燥管中盛装是的物质是
碱石灰
碱石灰
,作用是除去氢气中的水蒸气
除去氢气中的水蒸气
.(4)试管中收集气体是
H2
H2
,如果要在A处玻璃管处点燃该气体,则必须对该气体进行验纯
验纯
.分析:(1)Fe与水蒸气反应生成四氧化三铁和氢气,Fe元素的化合价升高,H元素的化合价降低;
(2)碎瓷片可防止暴沸发生;
(3)干燥管中的物质干燥氢气,除去氢气中的水蒸气;
(4)该反应生成氢气,为可燃性气体,点燃前应验纯.
(2)碎瓷片可防止暴沸发生;
(3)干燥管中的物质干燥氢气,除去氢气中的水蒸气;
(4)该反应生成氢气,为可燃性气体,点燃前应验纯.
解答:解:(1)Fe与水蒸气反应生成四氧化三铁和氢气,该反应为3Fe+4H2O(g)
Fe3O4+4H2↑,Fe元素的化合价升高,Fe为还原性,H元素的化合价降低,则水为氧化剂,故答案为:3Fe+4H2O(g)
Fe3O4+4H2↑;Fe;H2O;
(2)碎瓷片可防止暴沸发生,故答案为:防止暴沸;
(3)干燥管中的物质干燥氢气,则选碱石灰干燥剂来除去氢气中的水蒸气,故答案为:碱石灰;除去氢气中的水蒸气;
(4)该反应生成氢气,为可燃性气体,点燃前应验纯,否则气体不纯点燃会发生爆炸,故答案为:H2;验纯.
| ||
| ||
(2)碎瓷片可防止暴沸发生,故答案为:防止暴沸;
(3)干燥管中的物质干燥氢气,则选碱石灰干燥剂来除去氢气中的水蒸气,故答案为:碱石灰;除去氢气中的水蒸气;
(4)该反应生成氢气,为可燃性气体,点燃前应验纯,否则气体不纯点燃会发生爆炸,故答案为:H2;验纯.
点评:本题以铁与水的反应考查氧化还原反应,明确物质的性质及反应中元素的化合价变化即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案
相关题目
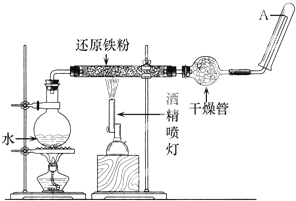 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验“. 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.