题目内容
【题目】A:已知C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

写出A的电子式_______;C的结构简式___________;
写出苯和液溴反应生成E的化学方程式_________________;
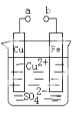
B.下图中的实验装置可用于制取乙炔请填空:

(1)图中,A管的作用是_______制取乙炔的化学方程式是____________________
(2)乙炔通入KMnO4酸性溶液中观察到的现象是_____________,乙炔发生了______________反应乙炔通入足量溴的CCl4溶液中反应的方程式是___________,在制取乙炔时常问道恶臭味这是因为实验中产生了H2S,PH3,ASH3等气体,请写出除去H2S杂质气体的离子方程式___________。
【答案】 H:C┇┇C:H ![]() C6H6 + Br2
C6H6 + Br2![]() C6H5Br + HBr 调节水面的高度来控制反应的发生和停止 CaC2+H2O
C6H5Br + HBr 调节水面的高度来控制反应的发生和停止 CaC2+H2O![]() Ca(OH)2+
Ca(OH)2+![]() ↑ 紫色酸性高锰酸钾溶液逐渐褪色 氧化 CH三CH+2Br2→CHBr2-CHBr2 H2S+Cu2+=CuS↓+2H+.
↑ 紫色酸性高锰酸钾溶液逐渐褪色 氧化 CH三CH+2Br2→CHBr2-CHBr2 H2S+Cu2+=CuS↓+2H+.
【解析】A、D是一种植物生长调节剂,用它可以催熟果实,则D为乙烯,气体A可以转化得到乙烯、苯,能与HCl发生加成反应,又碳化钙与水反应生成气体A,则A为乙炔,乙炔与HCl发生加成反应生成B,B发生反应生成合成树脂C,则B为CH2=CHCl,C为聚氯乙烯,苯与液溴在催化剂条件下发生取代反应生成E为![]() ;
;
(1)根据以上分析,A为乙炔,电子式为![]() ;D为乙烯,则C的结构简式为
;D为乙烯,则C的结构简式为![]() ;(2)苯和液溴反应生成E的化学方程式为:
;(2)苯和液溴反应生成E的化学方程式为:![]() +Br2
+Br2 ![]()
![]() +HBr。
+HBr。
B、(1)碳化钙和水的反应很剧烈,因此图中A管的作用是调节水面的高度来控制反应的发生和停止,实验室制取乙炔的化学方程式是CaC2+H2O→Ca(OH)2+HC≡CH↑;(2)乙炔含有碳碳三键,能把酸性高锰酸钾溶液氧化,则通入KMnO4酸性溶液中观察到的现象是紫色酸性高锰酸钾溶液逐渐褪色,其中乙炔发生了氧化反应;乙炔能与溴发生加成反应,因此乙炔通入足量溴的CCl4溶液中反应的方程式是CH≡CH+2Br2→CHBr2-CHBr2;H2S可以用硫酸铜溶液除去,反应的离子方程式为H2S+Cu2+=CuS↓+2H+。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】某温度下,0.200 molL-1的HA溶液与0.200 molL-1的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下表,下列说法正确的是
微粒 | X | Y | Na+ | A- |
浓度/(mol·L-1) | 8.00 | 2.50 | 0.100 | 9.92 |
A.0.1mol·L-1HA溶液的pH=1 B.该温度下Kw=1.0![]() 10-14
10-14
C.微粒X表示OH-,Y表示H+ D.混合溶液中:n(A-)+n(X)=n(Na+)