题目内容
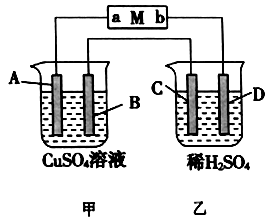
【题目】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将甲烷燃料电池作为电源,进行惰性电极电解饱和氯化钠溶液实验。回答下列问题:
(1)甲烷燃料电池正极的电极反应为_________、负极的电极反应为_________ 。
(2)如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。电解氯化钠溶液的离子反应方程式为_________。
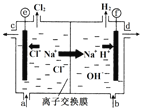
(3)精制饱和食盐水从图中_____位置补充,浓氢氧化钠溶液从图中______位置流出。(选填“a”、“b”、“c” 或“d”)
(4)若甲烷通入量为1L(标准状况),且反应完全,则最多能产生的氯气体积为______L(标准状况)
【答案】 2O2+4H2O+8e-=8OH- CH4+10OH--8e-=CO32-+7H2O 2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑ a d 4L
2OH-+Cl2↑+H2↑ a d 4L
【解析】试题分析:(1)在碱性溶液中,甲烷燃料电池的总反应式为CH4+2O2+2OH-=CO32-+3H2O,正极是:2O2+4H2O+8e-═8OH-,负极是:CH4-8e-+10OH-═CO32-+7H2O,故答案为:2O2+4H2O+8e-=8OH-;CH4+10OH--8e-=CO32-+7H2O;
(2)电解精制饱和食盐水的方法制取氯气、氢气、烧碱,反应的离子方程式为:2H2O+2Cl-![]() Cl2↑+2OH-+H2↑,故答案为:2H2O+2Cl-
Cl2↑+2OH-+H2↑,故答案为:2H2O+2Cl-![]() Cl2↑+2OH-+H2↑;
Cl2↑+2OH-+H2↑;
(3)电解槽中阴极是氢离子放电生成氢气,水电离平衡正向进行氢氧根离子浓度增大,生成氢氧化钠溶液,NaOH溶液的出口为d;Cl2在阳极,依据装置图分析可知精制饱和食盐水从阳极进入,即进口为a,故答案为:a,d;
(4)根据CH4-8e-+10OH-═CO32-+7H2O,若甲烷通入量为lL(标准状况),且反应完全,转移的电子的物质的量为![]() ×8=
×8=![]() mol,根据2H2O+2Cl-
mol,根据2H2O+2Cl-![]() Cl2↑+2OH-+H2↑,最多能产生标准状况下的氯气体积为
Cl2↑+2OH-+H2↑,最多能产生标准状况下的氯气体积为![]() mol ×
mol ×![]() ×22.4L/mol=4L,故答案为:4。
×22.4L/mol=4L,故答案为:4。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案