题目内容
【题目】按要求填空:
(1)写出下列物质的分子式:含6个碳原子的链状单烯烃__________________________。
(2)在戊烷的各种同分异构体中,一氯代物种类最多的键线式是_________________。
(3)用系统命名法命名 :______________
:______________
(4)某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个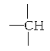 和一个-Cl。它的可能的结构有______________种
和一个-Cl。它的可能的结构有______________种
【答案】C6H12 ![]() 3,4-二甲基-4-乙基庚烷 4
3,4-二甲基-4-乙基庚烷 4
【解析】
(1)链状单烯烃通式为CnH2n;
(2)戊烷的同分异构体中,一氯代物种类最多的为异戊烷,键线式中只用键线来表示碳架,而分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略;
(3)依据烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小。看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号。如取代基不同,就把简单的写在前面,复杂的写在后面。
(4)C5H11Cl为戊烷的一氯代物,判断和书写烷烃的一氯代物的异构体可以按照以下步骤来做:先确定烷烃的碳链异构,即烷烃的同分异构体。 找出等效的氢原子。 根据先中心后两边的原则,将氯原子逐一去代替氢原子。据此判断符合条件的同分异构体数目。
(1)由于单烯烃的分子式通式是CnH2n,所以含6个碳原子的链状单烯烃的分子式是C6H12;(2)在戊烷的各种同分异构体中,一氯代物种类中正戊烷有3种,异戊烷有四种,新戊烷有一种,所以最多的是异戊烷,其键线式是![]() ;(3)根据有机物的系统命名法原则,化合物
;(3)根据有机物的系统命名法原则,化合物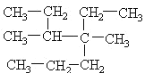 的名称是3,4-二甲基-4-乙基庚烷 ;(4)某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个
的名称是3,4-二甲基-4-乙基庚烷 ;(4)某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个-CH3、两个-CH2-、一个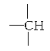 和一个-Cl。它的可能的结构有CH3CHCl-CH2CH2CH3、CH3CH2CHCl-CH2CH3、(CH3)2CHCH2CH2Cl、CH3CH2 CH (CH3) CH2Cl四种。
和一个-Cl。它的可能的结构有CH3CHCl-CH2CH2CH3、CH3CH2CHCl-CH2CH3、(CH3)2CHCH2CH2Cl、CH3CH2 CH (CH3) CH2Cl四种。

【题目】以辉铜矿为原料生产碱式碳酸铜的工艺流程如图所示:
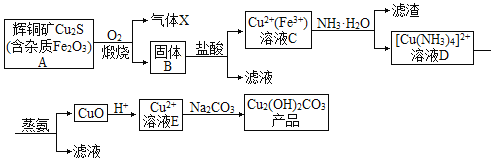
回答下列问题:
(1)若要提高辉铜矿煅烧效率可采取的措施有___(填两种)。
(2)气体X的主要成分是___(填化学式),写出该气体的一种用途___。
(3)蒸氨过程总反应的化学方程式是___。
(4)溶液E与Na2CO3溶液反应制取Cu2(OH)2CO3的离子反应方程式为___。
(5)某实验小组研究溶液E与Na2CO3溶液加料顺序及加料方式对产品的影响,实验结果如下:
实验序号 | 加料顺序及方式 | 沉淀颜色 | 沉淀品质 | 产率/% |
1 | 溶液E一次加入Na2CO3溶液中并迅速搅拌 | 浅蓝色 | 品质较好 | 87.8 |
2 | 溶液E逐滴加入Na2CO3溶液中并不断搅拌 | 暗蓝色 | 品质好 | 71.9 |
3 | Na2CO3溶液一次加入溶液E中并迅速搅拌 | 浅绿色 | 品质好 | 96.7 |
4 | Na2CO3溶液一次加入溶液E中并不断搅拌 | 浅蓝色 | 品质较好 | 102.7 |
由上表可知制取Cu2(OH)2CO3最佳加料顺序及加料方式是___(填序号)。
【题目】2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:CO2(g)+H2(g)![]() H2O(g) +CO(g) ΔH1 = +41.1 kJmol-1
H2O(g) +CO(g) ΔH1 = +41.1 kJmol-1
CO(g)+2H2(g)![]() CH3OH(g) ΔH2=-90.0 kJmol-1
CH3OH(g) ΔH2=-90.0 kJmol-1
则CO2催化氢化合成甲醇的热化学方程式:______________________。
(2)工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。判断反应达到平衡状态的依据是(填字母序号)________.
CH3OH(g)。判断反应达到平衡状态的依据是(填字母序号)________.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.混合气体的相对平均分子质量不变 D.CH3OH、CO、H2的浓度都不再发生变化
(3)如表所列数据是反应在不同温度下的化学平衡常数(K)
温度℃ | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
①该反应的化学平衡常数表达式为K=_____。
②由表中数据判断该反应的△H_____0(填“>”、“=”或“<”);
③某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则此时的温度为___________℃。
(4)要提高CO的转化率,可以采取的措施是(填字母序号)__________________.
a.增加CO的浓度 b.加入催化剂 c.升温 d.加入H2 e.加入惰性气体 f.分离出甲醇
(5)在一定条件下,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1体系中CO2的平衡转化率(
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1体系中CO2的平衡转化率(![]() )与L和X的关系如图所示,L和X分别表示温度或压强。
)与L和X的关系如图所示,L和X分别表示温度或压强。

①X表示的物理量是_____。
②判断L1与L2的大小关系:L1_____L2(填“<”,“=”或“>”),并简述理由:____________________。