题目内容
CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为( )
| A.25% | B.75% | C.88% | D.32% |
C
试题分析:设CO2和氢气的物质的量分别是x和y,则44x+2y=5g。氢气燃烧生成水,水和过氧化钠反应又生成氢氧化钠和氧气,反应的方程式可以看作是H2+Na2O2=2NaOH,所以该题增加的质量就是氢气的质量。根据方程式可知
2CO2+2Na2O2=2Na2CO3+O2 △m↑
2mol 56g
X 28x
所以28x+2y=3.4g
解得x=0.1mol
则CO2的质量设4.4g
所以CO2的质量分数是
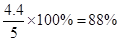
答案选C2、氢气混合燃烧通过过氧化钠的有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,针对性强,有利于考查学生灵活运用基础知识解决实际问题的能力。该题的关键是理解氢气燃烧后的生成物再和过氧化钠反应时,固体质量的变化规律。

练习册系列答案
相关题目
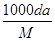
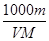
 %
%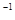 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看做是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )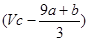 mol
mol
 与
与 离子总数为0.2NA
离子总数为0.2NA