题目内容
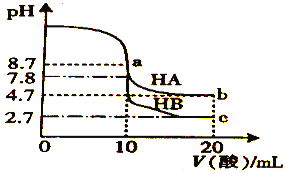
【题目】常温下,分别向10 mL 0.1 molL1的NaOH 溶液中逐滴加入0.1 molL1的一元酸HA和HB溶液,用pH传感器测得混合溶液的pH变化曲线如图所示,下列说法正确的是
A. HA的酸性强于HB的酸性
B. V(酸)=10mL时,两份溶液中c(B)=c(A)
C. a 点时,c(A)>c(Na+)>c(OH)>c(H+)
D. b、c点时,c(A)+c(HA)=2c(Na+)=c(HB)+c(B)
【答案】D
【解析】A项,当V(酸)=10mL时,酸碱恰好完全反应得到等物质的量浓度的NaA溶液、NaB溶液,NaA溶液的pH大于NaB溶液的pH,HA的酸性弱于HB的酸性;B项,V(酸)=10mL时,酸碱恰好完全反应得到等物质的量浓度的NaA溶液、NaB溶液,NaA溶液的pH大于NaB溶液的pH,A-的水解能力大于B-的水解能力,两溶液中c(B-)![]() c(A-);C项,a点为NaA溶液,由于A-的水解溶液呈碱性,溶液中离子浓度由大到小的顺序为c(Na+)
c(A-);C项,a点为NaA溶液,由于A-的水解溶液呈碱性,溶液中离子浓度由大到小的顺序为c(Na+)![]() c(A-)
c(A-)![]() c(OH-)
c(OH-)![]() c(H+);D项,b点为等浓度的NaA和HA的混合液,c点为等浓度的NaB和HB的混合液,根据物料守恒作答。
c(H+);D项,b点为等浓度的NaA和HA的混合液,c点为等浓度的NaB和HB的混合液,根据物料守恒作答。
A项,当V(酸)=10mL时,酸碱恰好完全反应得到等物质的量浓度的NaA溶液、NaB溶液,NaA溶液的pH(8.7)大于NaB溶液的pH(7.8),根据盐类水解的规律“越弱越水解”,HA的酸性弱于HB的酸性,A项错误;B项,V(酸)=10mL时,酸碱恰好完全反应得到等物质的量浓度的NaA溶液、NaB溶液,NaA溶液的pH大于NaB溶液的pH,A-的水解能力大于B-的水解能力,两溶液中c(B-)![]() c(A-),B项错误;C项,a点加入10mL的HA溶液,得到NaA溶液的pH=8.7,由于A-的水解溶液呈碱性,溶液中离子浓度由大到小的顺序为c(Na+)
c(A-),B项错误;C项,a点加入10mL的HA溶液,得到NaA溶液的pH=8.7,由于A-的水解溶液呈碱性,溶液中离子浓度由大到小的顺序为c(Na+)![]() c(A-)
c(A-)![]() c(OH-)
c(OH-)![]() c(H+),C项错误;D项,b点加入20mL的HA溶液得到等浓度的NaA和HA的混合液,溶液中的物料守恒为c(A-)+c(HA)=2c(Na+),c点加入20mL的HB溶液得到等浓度的NaB和HB的混合液,溶液中的物料守恒为c(B-)+c(HB)=2c(Na+),b、c两点溶液中c(Na+)相等,则c(A-)+c(HA)=2c(Na+)= c(B-)+c(HB),D项正确;答案选D。
c(H+),C项错误;D项,b点加入20mL的HA溶液得到等浓度的NaA和HA的混合液,溶液中的物料守恒为c(A-)+c(HA)=2c(Na+),c点加入20mL的HB溶液得到等浓度的NaB和HB的混合液,溶液中的物料守恒为c(B-)+c(HB)=2c(Na+),b、c两点溶液中c(Na+)相等,则c(A-)+c(HA)=2c(Na+)= c(B-)+c(HB),D项正确;答案选D。

【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为_____。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____(填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______(填化学式)。
(4)元素②、⑤形成化合物的电子式为_____。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
【题目】如表为周期表中短周期的一部分,若X原子的最外层电子数是Y原子内层电子总数的![]() ,则下列说法不正确的是
,则下列说法不正确的是![]()
![]()
W |
|
|
|
| X | Y | Z |
A. Y的最高价氧化物的水化物的酸性比X的强 B. W、Z组成的某化合物是一种常见的溶剂
C. 原子半径大小比较:![]() D. W形成的氢化物种类很多
D. W形成的氢化物种类很多