题目内容
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列
有关说法正确的是( )
有关说法正确的是( )
| A.除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
| B.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强 |
| C.因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生 |
| D.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L |
A
试题分析:A.FeS、CuS的溶度积常数(Ksp)分别为6.3×10﹣18、1.3×10﹣36.FeS溶度积大于CuS溶度积,所以除去工业废水中的Cu2+可以选用FeS作沉淀剂,故A正确;B.根据H2S与SO2反应生成单质硫和水,硫化氢被反应掉了,浓度减小,酸性减弱,故B错误;C.CuS是不溶于酸的黑色物质,所以能发生反应:CuSO4+H2S═CuS↓+H2SO4,这是弱酸制备强酸的特例,故C错误;D.H2S是弱酸,硫离子的最大浓度为0.1 mol/L,CuS的溶度积常数(Ksp)为1.3×10﹣36,所以溶液中Cu2+的最小浓度为1.3×10﹣35 mol/L,故D错误;故选:A。

练习册系列答案
相关题目

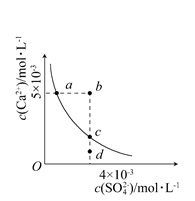
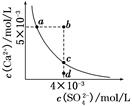

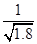 ×10—11mol?L—1
×10—11mol?L—1 Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为
Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为