题目内容
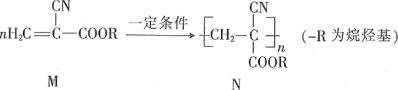
【题目】一定温度下,在2L的恒容密闭容器中发生反应A(g)+2B(g)![]() 3C(g)。反应过程中的部分数据如下表所示:
3C(g)。反应过程中的部分数据如下表所示:
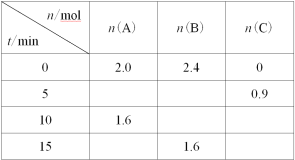
下列说法正确的是( )
A.0~5min用A表示的平均反应速率为0.09mol·L1·min1
B.该反应在10min后才达到平衡
C.平衡状态时,c(C)=0.6mol·L1
D.物质B的平衡转化率为20%
【答案】C
【解析】
发生的反应为:
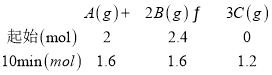
15min时,n(B)=1.6mol,与10min时数据一致,说明反应已经达到平衡,据此逐项分析。
A.0~5 min内,△n(C)=0.9mol,根据方程式,则△n(A)=![]() △n(C)=0.3mol,所以用A表示的平均反应速率为v(A)=
△n(C)=0.3mol,所以用A表示的平均反应速率为v(A)=![]() =
=![]() =
=![]() =0.03mol/(Lmin),选项A错误;
=0.03mol/(Lmin),选项A错误;
B.反应在10min时,B变化了0.8mol,则此时B余下1.6mol,到15min时,B仍然是1.6mol,说明反应在10min已经达到平衡,选项B错误;
C.15min时,n(B)=1.6mol,与10min时数据一致,说明反应在10min已经达到平衡,则平衡时,c(C)=![]() =0.6mol/L,选项C正确;
=0.6mol/L,选项C正确;
D.物质B的转化率为α(B)=![]() ×100%=33.3%,选项D错误;
×100%=33.3%,选项D错误;
答案为A。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案【题目】已知:① X、Y、Z、W、R、Q为原子序数依次增大的短周期元素。X 是所有元素中原子半径最小的元素,Y是形成化合物种类最多的元素,W的最外层电子数是次外层电子数的3倍,Q与W同主族,Y、R原子的最外层电子数之和等于Z的最外层电子数。
②莱纳斯·卡尔·鲍林在1932年提出electronegativity作为元素原子在化合物某种性质的标度,electronegativity的大小可以判断元素金属性与非金属性强弱,下表列出部分短周期元素的Electronegativity的值。
元素 | X | Y | Z | W | R | Q |
electronegativity | 2.1 | 2.5 | 3.0 | 3.5 | 0.9 | 2.5 |
元素 | Mg | Li | Al | Cl | P | Be |
electronegativity | 1.2 | 1.0 | 1.5 | 3.0 | 2.1 | 1.5 |
请回答下列问题(涉及X、Y、Z、W、R、Q时,用元素符号表示):
(1)根据上表给出的数据,可知元素的electronegativity越大,__(填“金属性”或“非金属性”)越强。
(2)元素Q在周期表中的位置为_________。
(3)W、R、Q单核简单离子半径由大到小排列顺序为______。
(4)元素X、Z、W之间能形成多种10电子微粒,请写出反应物和产物均为X、Z、W之间形成的10电子微粒的一个离子方程式______________。
(5)一种由元素W、R组成的白色固体化合物,其电子式为_______________。
(6)试比较稳定性:X2W_____ X2Q;沸点:X2W_____ X2Q (填“<”或“>”)。
(7)元素 X、Y、Z、W、R、Q中的两种元素可形成原子个数比为1∶2的共价化合物,则这两种元素的原子序数之差不可能是_________。
A.2 B.4 C.5 D.7