题目内容
【题目】如图为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述中不正确的是( )
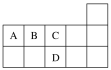
A.A、C两元素形成的化合物都为共价化合物
B.AD2的电子式为![]()
C.B2的结构式为N≡N
D.B、C形成的化合物BC中所含化学键为非极性共价键
【答案】D
【解析】
根据图示分析,A为C,B为N,C为O,D为S。
A. A、C两元素形成的化合物为非金属元素之间形成的碳氧化合物,都为共价化合物,A正确;
B. CS2中C的最外层电子数为4,要形成4对共用电子对,S的最外层电子数为6,要形成2对共用电子对,2个S形成2对,其的电子式为![]() ,B正确;
,B正确;
C. N2的结构式为N≡N,C正确;
D. B、C形成的化合物为NO,N、O原子不同,共用电子对发生偏移,所含化学键为极性共价键,D错误。
答案选D。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】现有部分短周期元素的性质或原子结构如表:
元素编号 | 元素的性质或原子结构 |
X | 最外层电子数是次外层电子数的3倍 |
Y | 常温下单质是双原子分子,其氢化物的水溶液显碱性 |
Z | 第三周期元素的简单离子中半径最小 |
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是________,元素Z的离子结构示意图为________。
(2)元素Y与氢元素形成一种离子YH![]() ,请写出该离子电子式 __________________。
,请写出该离子电子式 __________________。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:
___________________________________。
(4)元素X与元素Y相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.X的单质比Y的单质更容易与H2化合
c.X与Y形成的化合物中Y元素呈正价态
【题目】氨气是工农业生产中不可或缺的物质,研究制取氨气的机理意义非凡。
(1)在常温、常压、光照条件下,N2在掺有少量Fe2O3的TiO2催化剂表面与水发生下列反应:
N2(g)+3H2O(l)![]() 2NH3(g)+3/2O2(g) △H= a kJ mol-1。
2NH3(g)+3/2O2(g) △H= a kJ mol-1。
为进一步研究生成NH3的物质的量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
n(NH3)/(l0-2mol) | 4.8 | 5.9 | 6.0 |
此反应的a_________0,△S________0。(填“>”“<”或“ = ”)
(2)—定温度和压强下,在2 L的恒容密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
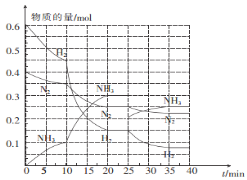
①0~10 min内,以NH3表示的平均反应速率为_________。
②在10~20 min内,NH3浓度变化的原因可能是_______。
A.加入催化剂 B.缩小容器体积 C.降低温度 D.增加NH3的物质的量
③ 20 min达到第一次平衡,在反应进行至25 min时,曲线发生变化的原因是____________,35min达到第二次平衡,则平衡的平衡常数K1______K2(填“>”“<”或“ = ”)