题目内容
【题目】现有部分短周期元素的性质或原子结构如表:
元素编号 | 元素的性质或原子结构 |
X | 最外层电子数是次外层电子数的3倍 |
Y | 常温下单质是双原子分子,其氢化物的水溶液显碱性 |
Z | 第三周期元素的简单离子中半径最小 |
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是________,元素Z的离子结构示意图为________。
(2)元素Y与氢元素形成一种离子YH![]() ,请写出该离子电子式 __________________。
,请写出该离子电子式 __________________。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:
___________________________________。
(4)元素X与元素Y相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.X的单质比Y的单质更容易与H2化合
c.X与Y形成的化合物中Y元素呈正价态
【答案】O3 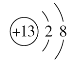
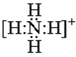
![]() O abc
O abc
【解析】
短周期元素中,最外层电子数是次外层电子数的3倍,则X为氧元素;常温下单质为双原子分子,其氢化物水溶液呈碱性,则Y为氮元素;第三周期元素的简单离子中半径最小,则Z为铝元素,据此解答。
(1)氧元素的单质O3具有强氧化性,可在生活中常用作饮水机的消毒剂;铝离子的质子数为13,核外电子数为10,其结构示意图为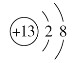 ;
;
(2)![]() 中N原子与H原子之间均存在一对共用电子对,其电子式为:
中N原子与H原子之间均存在一对共用电子对,其电子式为: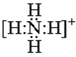 ;
;
(3)Z元素最高价氧化物对应的水化物为Al(OH)3,Al(OH)3与NaOH的反应为:Al(OH)3+NaOH=NaAlO2+2H2O,离子反应为:![]() ;
;
(4)因N、O元素处于同周期,同周期随原子序数的增大,非金属逐渐增强,故O元素的非金属强;a中的氧化还原反应可判断氧气的氧化性大于氮气的氧化性,则氧的非金属性大于氮元素的非金属性,b中与氢气的化合的难易程度可知氧的非金属性强,c中氧元素比氮元素容易得到电子,则氧的非金属强,故答案为:O;abc。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案